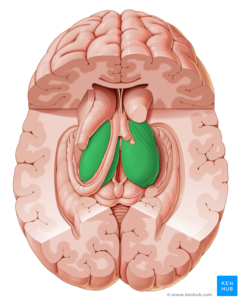
Il talamo è una struttura ovoidale pari del diencefalo di cui costituisce il maggior organo. Embriologicamente deriva dal diencefalo, a sua volta formatosi dal prosencefalo alla 5-6a settimana di gravidanza. Il suo volume aumenta dalla 19a settimana fino a termine di gravidanza quando raggiunge una lunghezza di circa 4 cm, larghezza 1.5 cm e altezza (diametro trasverso) 2.5 cm . Una mancata crescita delle dimensioni talamiche può provocare problemi psichiatrici o autismo.

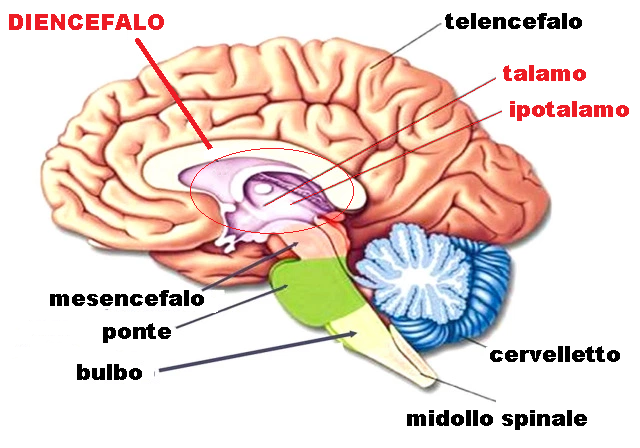
E’ situato a livello della base cranica, sopra il mesencefalo e al di sotto del corpo calloso, bilateralmente ai margini laterali del terzo ventricolo e insieme a questo, all’ipotalamo e epitalamo forma il diencefalo.
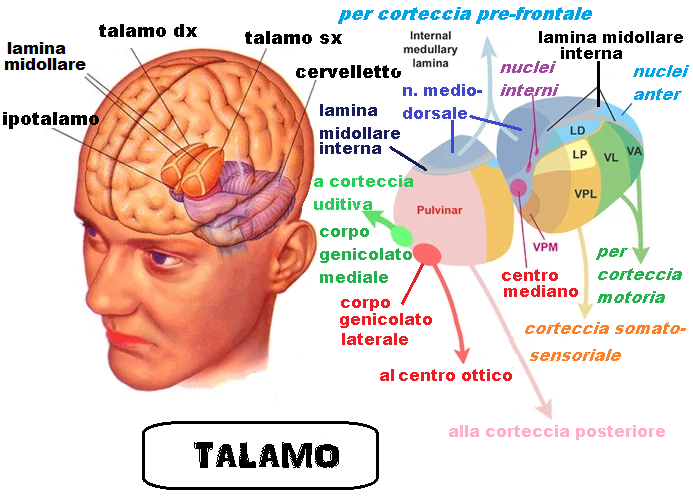
Le due strutture talamiche sono fra di loro collegate tramite la commissura intertalamica. Il talamo è composto da circa 50 nuclei distinti in base alla loro collazione all’interno dell’ovoide e in rapporto alla lamina midollare interna: anteriori, laterali, mediali e posteriori. Inoltre al talamo appartengono anche due protuberanze della parte posteriore denominati corpi genicolati mediale e laterale.
 E’ irrorato da alcune branche dell’a. cerebrale posteriore che è uno dei vasi che compongono il circolo di Willis.
E’ irrorato da alcune branche dell’a. cerebrale posteriore che è uno dei vasi che compongono il circolo di Willis.
Possiamo descrivere 4 facce del talamo:
- la faccia superiore delimitata dalla stria midollare del talamo e il solco opto-striato formazioni che lo separano dal nucleo caudato, dal fornice e dal pavimento della cella media del ventricolo laterale;
- la faccia mediale costituisce la parete laterale del terzo ventricolo;
- la faccia inferiore è in rapporto con l’ipotalamo tramite interposizione del solco ipotalamico (di Monro);
- la faccia laterale è separata tramite la capsula interna (braccio posteriore) dal nucleo lenticolare;
Il polo anteriore del talamo in rapporto con il fornice delimita il foro interventricolare di Monro, che collega i primi due ventricoli con il terzo; il polo posteriore si prolunga in basso sotto il crocicchio del ventricolo laterale formando il nucleo genicolato mediale e il nucleo genicolato laterale.
Macroscopicamente si presenta come un ovoide, orientato in senso medio-laterale dall’anteriore al  posteriore, lungo circa 4 cm, largo 1.5 cm e alto 2.5 cm. Il talamo è un ammasso di sostanza grigia, con sostanza bianca nello strato zonale che ne riveste la superficie superiore e nelle lamine midollari interna ed esterna. La lamina midollare interna si biforca anteriormente a Y e in rapporto ad essa noi suddividiamo i nuclei talamici in nuclei anteriori (compresi nella biforcazione), nuclei mediali e nuclei laterali. I nuclei laterali vengono distinti in dorsali e ventrali. Inoltre vi sono i nuclei intralaminari nello spessore della lamina midollare interna, di cui il più grande è il nucleo centro-mediano (CM), il nucleo reticolare posto lungo la superficie laterale del talamo e i nuclei della linea mediana del talamo posti sulla superficie mediale dello stesso. La lamina midollare esterna separa il nucleo reticolare dal resto della sostanza grigia talamica.
posteriore, lungo circa 4 cm, largo 1.5 cm e alto 2.5 cm. Il talamo è un ammasso di sostanza grigia, con sostanza bianca nello strato zonale che ne riveste la superficie superiore e nelle lamine midollari interna ed esterna. La lamina midollare interna si biforca anteriormente a Y e in rapporto ad essa noi suddividiamo i nuclei talamici in nuclei anteriori (compresi nella biforcazione), nuclei mediali e nuclei laterali. I nuclei laterali vengono distinti in dorsali e ventrali. Inoltre vi sono i nuclei intralaminari nello spessore della lamina midollare interna, di cui il più grande è il nucleo centro-mediano (CM), il nucleo reticolare posto lungo la superficie laterale del talamo e i nuclei della linea mediana del talamo posti sulla superficie mediale dello stesso. La lamina midollare esterna separa il nucleo reticolare dal resto della sostanza grigia talamica.
Nuclei talamici anteriori
I nuclei talamici anteriori sono compresi all’interno della biforcazione della Y della lamina midollare interna del talamo, inferiormente al tubercolo talamico anteriore. Si distinguono il nucleo antero-dorsale e il nucleo antero-mediale. Le afferenze principali ai nuclei talamici anteriori sono costituite dal tratto mammillo-talamico. Il corpo mammillare mediale proietta al nucleo anteromediale e il nucleo mammillare laterale proietta al nucleo antero-dorsale. Oltre al tratto mammillo-talamico questi nuclei ricevono afferenze colinergiche dal tronco encefalico. Le efferenze sono costituite da fibre che proiettano al giro para-ippocampico (parte del sistema limbico), al giro del cingolo e alla corteccia limbica anteriore. Come per tutte le proiezioni talamo-corticali, esistono parimenti proiezioni corticotalamiche reciproche. Si ritiene che questi nuclei siano coinvolti nell’acquisizione della memoria e nella regolazione dello stato d’allerta.
Nuclei talamici mediali
I nuclei talamici mediali sono costituiti dal nucleo mediodorsale e da altri sei nuclei collocati sulla linea mediana, i quali ricevono afferenze dal tronco cerebrale e proiettano diffusamente verso la corteccia cerebrale, l’amigdala e nuclei della base. Il nucleo mediodorsale collocato tra i nuclei della linea mediana e la lamina midollare interna, forma gran parte della porzione mediale del talamo. Il nucleo dorsomediale (MD) è diviso a sua volta in una parte mediale a grandi cellule (magnocellulare) e una parte dorsolaterale a piccole cellule (parvocellulare), più una parte aderente alla lamina midollare interna (paralaminare). La porzione magnocellulare riceve afferenze olfattive dalla corteccia piriforme e dall’amigdala; le sue proiezioni sono dirette al lobo frontale e alla corteccia prefrontale, in particolare a quelle strutture coinvolte nella percezione olfattiva, altre raggiungono il giro del cingolo e l’insula. La componente parvocellulare, più rappresentata in questo nucleo e collocata posteriormente, è connessa alla corteccia prefrontale, con il giro del cingolo e con la corteccia motoria supplementare. Le sue fibre efferenti si  portano alla corteccia parietale posteriore. Il nucleo mediodorsale paralaminare si ritiene abbia un ruolo nel movimento oculare e nella percezione del dolore. L’atrofia del n. dorso-mediale sono caratteristici della Sindrome di Wernicke-Korsakoff.
portano alla corteccia parietale posteriore. Il nucleo mediodorsale paralaminare si ritiene abbia un ruolo nel movimento oculare e nella percezione del dolore. L’atrofia del n. dorso-mediale sono caratteristici della Sindrome di Wernicke-Korsakoff.
Nuclei talamici laterali
Il nucleo laterale dorsale (LD) riceve afferenze dal pretetto e dal collicolo superiore. Esso è connesso con le cortecce cingolata, retrosplenica e paraippocampale posteriore, con la corteccia parietale e con il presubiculum della formazione ippocampale.
Il nucleo laterale posteriore (LP) si trova in continuità con il nucleo LD, dorsalmente al nucleo ventrale posteriore. Si connette reciprocamente con il lobo parietale superiore e le sue afferenze sottocorticali derivano dal collicolo superiore.
Il nucleo caudale, o pulvinar, è il maggiore dei nuclei talamici, si trova tra il nucleo genicolato laterale e il nucleo genicolato mediale e rappresenta la stazione di collegamento per la via visiva extragenicolata.
Il nucleo ventrale anteriore (VA) riceve gli impulsi dall’area motoria soppressoria (4s) tramite il globus pallidus che riceve fibre dal corpo striato; è connesso anche con il putamen da fibre per l’area motrice primaria e secondaria (aree 4 e 6) con funzione soppressoria.
Il nucleo ventrale laterale (VL) connette la corteccia cerebellare con la corteccia cerebrale tramite le fibre cerebello-rubre-talamiche e cerebello-talamiche e inviando fibre alle aree motrice primaria e secondaria.
Il nucleo ventrale posteriore (VP) è formato dal nucleo posterolaterale (VPL) intercalato alle vie sensitive quali quelle del lemnisco mediale e dei fasci spino-talamici anteriori e laterali i quali costituiscono il lemnisco spinale, e dal nucleo posteromediale (VPM) da cui passano le vie del lemnisco trigeminale, del lemnisco viscerale, delle fibre bulbo-talamiche e, nella parte più mediale le vie per l’informazione gustativa dirette alla cresta dell’insula; insieme, questi due nuclei contengono una rappresentazione topografica completa del corpo. Da questo nucleo partono fibre che partecipano alla radiazione sensitiva che si porta all’area sensitiva primaria.
I nuclei mediali sono connessi con l’ipotalamo periventricolare e la corteccia prefrontale e riceve afferenze dal nucleo ventrale posteriore.
Altri nuclei talamici
Dei nuclei intralaminari, i più voluminosi sono i nuclei centromediani (CM), che ricevono afferenze dalla corteccia motoria primaria, dai nuclei della base e dalla formazione reticolare, e i nuclei parafascicolari (Pf), che ricevono afferenze dalla corteccia premotoria. Si ritiene che questi nuclei integrino le informazioni corticali e subcorticali del movimento.
Il nucleo reticolare e quelli della linea mediana ricevono afferenze dalla formazione reticolare.
Funzioni dell’ipotalamo: importante ruolo di trasmissione e modulazioni tonica o fasica degli stimoli motori e sensitivi.
- il talamo rappresenta un centro intercalato sulle vie della sensibilità somatica, con funzioni di integrazione e di “arricchimento”, grazie alle connessioni col sistema limbico, il quale trasporta contenuti emozionali della percezione sensitiva.
- Regola la componente motoria grazie ai circuiti pallido-talamo-corticale (sistema extrapiramidale) e cerebello-talamo-corticale (regolazione del tono muscolare).
- Attiva la corteccia cerebrale.
- Il pulvinar interviene nello schema corporeo (coscienza globale del corpo)
- Il corpo genicolato mediale è un centro di collegamento per la funzione uditiva
- il genicolato laterale riceve la via ottica e invia fibre alla radiazione ottica
References:
- Tyler J. Torrico; Sunil Munakomi: Neuroanatomy, Thalamus. StatPearls [Internet], 2022.
- Herrero M‐T, Barcia C, Navarro J. Functional anatomy of thalamus and basal ganglia. Childs Nerv Syst 2002; 18(8): 386–404.
- Benavides-Serralde A, Hernández-Andrade E, Fernández-Delgado J, Plasencia W, Scheier M, Crispi F, Figueras F, Nicolaides KH, Gratacós E. Three-dimensional sonographic calculation of the volume of intracranial structures in growth-restricted and appropriate-for-gestational age fetuses. Ultrasound Obstet Gynecol. 2009 May;33(5):530-7
- Stein T, Moritz C, Quigley M, Cordes D, Haughton V, Meyerand E. Functional connectivity in the thalamus and hippocampus studied with functional MR imaging. AJNR Am J Neuroradiol. 2000 Sep;21(8):1397-401.
- Child ND, Benarroch EE. Anterior nucleus of the thalamus: functional organization and clinical implications. Neurology. 2013 Nov 19;81(21):1869-76.