Ultimo aggiornamento 16/09/2023
Con il termine diabete sono comprese alcune malattie, differenti per eziologia, patogenesi e decorso clinico, ma aventi come denominatore comune il sintomo di iperglicemia persistente a digiuno (>110 mg/dl; v.n.  normale 70-110 mg/dl) associata a poliuria e glicosuria.
normale 70-110 mg/dl) associata a poliuria e glicosuria.
Provoca notevoli alterazioni metaboliche che portano a complicanze del sistema circolatorio, nervoso, renale e apparato oculare.
CLASSIFICAZIONE DEL DIABETE –
Il diabete può essere classificato anzitutto in primario insulino dipendente (IDDM) e primario non insulino dipendente (NIDDM) e secondario a pancreatiti, pancreasectomia, modificazioni strutturali insuliniche, modificazioni dei recettori dell’insulina.
Un’altra classificazione suddivide la patologia in 3 tipi: I, II, III. Il diabete di tipo I rappresenta il 5% delle forme di diabete; è una malattia autoimmune che richiede l’uso quotidiano di insulina. I sintomi del diabete di tipo I più frequentemente osservati sono polidipsia, poliuria, attacchi di fame (in relazione alle crisi ipoglicemiche), perdita di peso, disturbi della vista e stanchezza cronica.
Il diabete di tipo II è la forma più comune di diabete rappresentando il 90-95% dei casi di diabete. I sintomi di questa patologia sono rappresentati da frequenti infezioni urinarie, aumento della sete e della minzione, costante fame e facile affaticabilità. Questa forma di diabete è spesso associata con l’età avanzata, l’obesità, anamnesi familiare positiva, precedente diabete gestazionale, inattività fisica, patologie epatiche.
Il diabete di tipo III, detto anche diabete gestazionale (GDM, Gestational diabetes mellitus), è, secondo la definizione del WHO, “intolleranza al glucosio che si manifesta durante la gravidanza e che scompare dopo il parto”.
Tutte le donne in gravidanza manifestano un certo di grado di resistenza all’insulina, ma nella maggior parte dei casi l’organismo riesce a supplire aumentandone la produzione. Il diabete gestazionale insorge più frequentemente fra la 24a e la 28a settimana di gestazione e si manifesta con valori di glicemia basale >120-140 mg/dl o per valori glicemici >180 mg/dl al 60′ di una minicurva da carico di glucosio. Interessa il 5% delle donne gravide <25 anni e il 20% delle gravide >35 anni. In genere si tratta di pazienti ad alto rischio di diabete o addirittura pre-diabetiche che non riescono a compensare la fisiologica iperglicemia gravidica con adeguato incremento insulinico (1). Queste pazienti presentano un alto rischio di sviluppare in seguito un diabete di tipo 2. Anche i loro figli sono ad alto rischio per diabete di tipo 2 e per obesità. Tali pazienti perciò vanno monitorate per il diabete tipo II per tutta la vita.
Se il diabete era già presente in epoca precedente alla gravidanza, si parla di diabete in gravidanza.
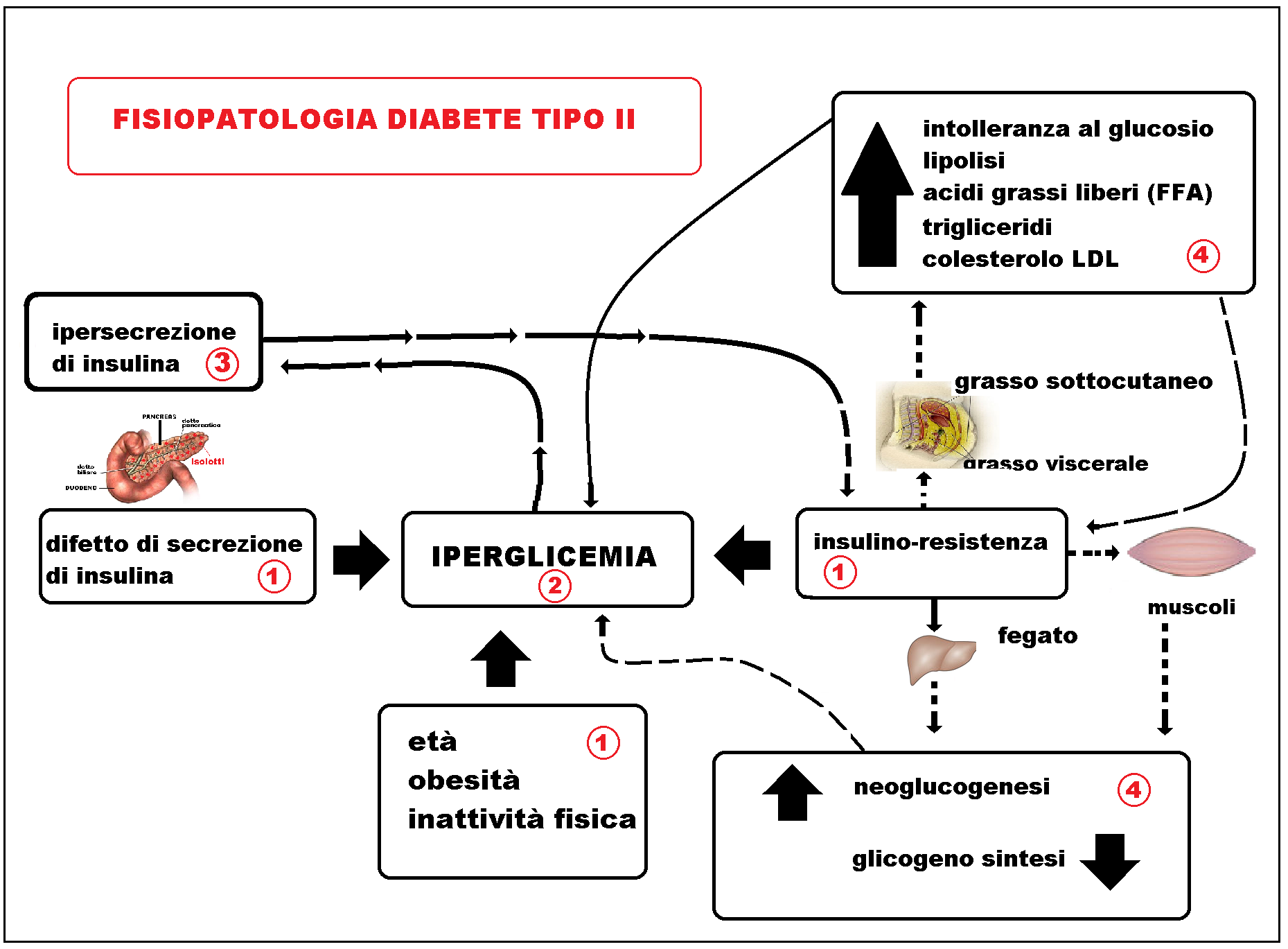
FISIOPATOLOGIA DEL DIABETE TIPO II
Nella patogenesi del diabete mellito tipo 2 si riconoscono tre alterazioni fisiopatologiche fondamentali:
- un difetto relativo di secrezione insulinica;
- uno stato di insulino-resistenza a livello del tessuto muscolare e adiposo;
- uno stato di insulino-resistenza a livello epatico (con conseguente aumentata gluconeogenesi e alterata sintesi del glicogeno ).
L’insulino-resistenza è una condizione presente nel diabete mellito tipo 2 ed è il risultato dell’interazione di fattori genetici e fattori ambientali (attività fisica, alimentazione, età).
L’obesità è uno dei principali fattori predisponenti per il diabete mellito tipo 2 inducendo insulino-resistenza e alterazioni metaboliche (alterata tolleranza al glucosio, ipertrigliceridemia e bassi livelli di colesterolo HDL), obesità centrale (in particolare viscerale), ipertensione arteriosa, microalbuminuria, disfunzione endoteliale, alterazioni del sistema coagulativo e fibrinolitico, iperuricemia, infiammazione. Tutti questi fattori confluiscono nella sindrome metabolica.
Il difetto dell’azione dell’insulina si esplica a livello dei tessuti periferici: muscolo e tessuto adiposo. A livello del tessuto muscolare la capacità dell’insulina promuove l’utilizzazione di glucosio e il suo immagazzinamento in forma di glicogeno; queste azioni sono ridotte e contribuiscono all’iperglicemia della fase post-prandiale.
A livello del tessuto adiposo la resistenza all’insulina si traduce in una ridotta utilizzazione di glucosio e in un aumento della lipolisi con elevazione degli acidi grassi liberi (FFA) circolanti. L’aumentato afflusso di acidi grassi contribuisce all’insulino-resistenza a livello del tessuto muscolare.
Elevate concentrazioni di acidi grassi liberi, insulino-resistenza epatica e un eccesso di glucagone comportano un’aumentata attività gluconeogenetica epatica che mantiene un eccesso di produzione di glucosio da parte del fegato in condizione basale e un’assente soppressione nelle fasi post-prandiali.
Una franca iperglicemia (diabete) si manifesta qualora sia presente un difetto nella secrezione insulinica. Nelle fasi iniziali della malattia diabetica in risposta allo stato di insulino-resistenza, un aumento compensatorio della secrezione insulinica delle cellule pancreatiche mantiene nella norma livelli circolanti di glicemia. Con il progredire della malattia la secrezione pancreatica di insulina si riduce causando iperglicemia. Un aumento dei livelli del glucosio ematico nelle fasi iniziali della malattia soprattutto nel periodo post-prandiale dato che il muscolo scheletrico rappresenta una tappa fondamentale nell’utilizzo dei carboidrati ingeriti con il pasto e nelle fasi più avanzate, anche a digiuno quando la produzione epatica di glucosio non risulta più sufficientemente soppressa. Il progressivo aumento della glicemia ha un ruolo importante nel favorire la progressione dell’insulino resistenza e del difetto di secrezione (glucotossicità) instaurandosi così un circolo vizioso.
In ultima analisi il diabete mellito tipo 2 rappresenta il risultato di alterazioni fisiopatologiche riscontrabili a livello di vari organi: insulino-resistenza del tessuto muscolare e adiposo, ridotta secrezione insulinica a livello delle beta-cellule pancreatiche, iperproduzione epatica di glucosio non più inibita dall’azione insulinica.
Tutte queste alterazioni fisiopatologiche si embricano tra loro e sono alla base dell’iperglicemia, e come tali sono i principali “obiettivi” della terapia del diabete mellito tipo 2.
SINTOMATOLOGIA
- Polidipsia: sete intensa per cui si tende a bere >3 litri di acqua al dì poliuria: diuresi >2.5 lt/die
- perdita di peso.
- vomito da neuropatia del sistema nervoso autonomo (accumulo di glucosio-sorbitolo e rigonfiamento e rottura della membrana di Schwam): nelle gravide diabetiche il vomito può avere conseguenze disastrose sul feto per il quale la chetoacidosi o acidosi metabolica può essere fatale in qualsiasi momento della gravidanza. Addirittura c’è pericolo che i chetoni prodotti in corso di vomito possano danneggiare il feto anche in assenza di chetoacidosi.
- candidosi ricorrenti e ribelli alle terapie
- Cistiti ricorrenti
- Restless legs syndrome
- diminuzione dell’acuità visiva da microangiopatia retinica
- Insulti ischemici a livello coronarico, cerebrale e degli arti inferiori e superiori
- Obesità e/o distribuzione prevalentemente viscerale dell’adipe.
DIAGNOSTICA DI LABORATORIO:
►glicemia basale: >140 mg/dl, pone senza dubbio alcuno la diagnosi di diabete mellito.
► Insulino-resistenza: glicemia/insulinemia <5
►Curva da carico di glucosio (OGTT, Oral Glucose Tolerance Test): da eseguire in tutte le gravide di età superiore ai 30 anni o a rischio di DG. E’ preferibile utilizzare la cosiddetta minicurva: 75 gr di glucosio per os diluito in 200 cc di acqua da bere in 5 minuti; la glicemia presenta una curva bifasica: rialzo iniziale seguito da lento rientro nei valori basali entro 2 ore dopo l’assunzione di glucosio.
►Emoglobina glicosilata (HbA1c): è un indice delle glicemia nei 3-4 mesi precedenti. Correlata al rischio di malformazioni fetali. Valori di HbA1c <7% sono indicativi di un andamento glicemico adeguato. Se, al contrario, i valori sono superiori all’8% è necessaria una modifica del trattamento terapeutico.
►C-Peptide – polipeptide costituito da 31 aminoacidi, posto fra a collegamento fra la catena α e la catena ß della proinsulina. Si libera nel processo di trasformazione, scissione enzimatica, della pro-insulina in insulina.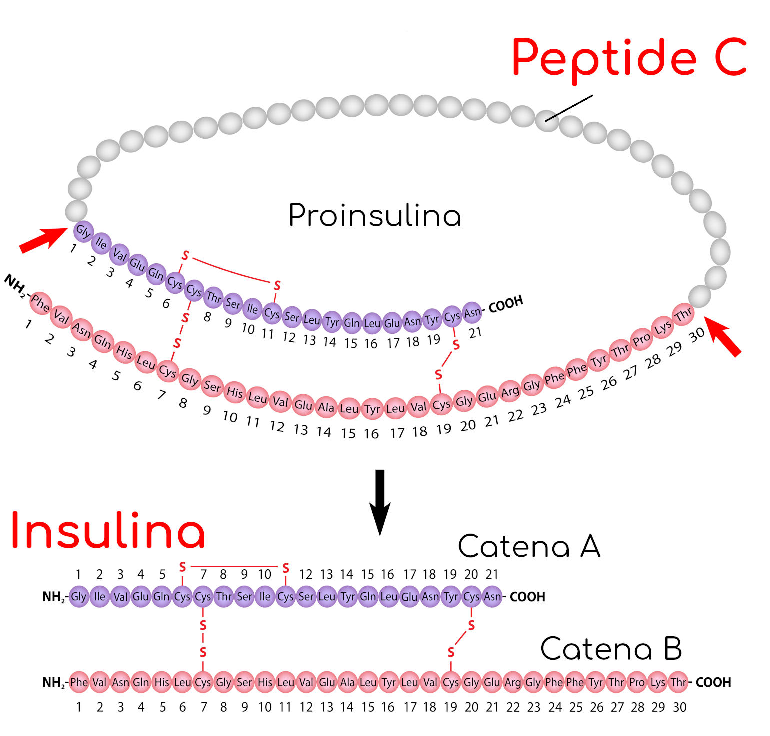
In conseguenza di questo processo insulina e C-peptide sono immessi in circolo in uguale concentrazione. Il dosaggio del C-peptide è quindi un buon indicatore della secrezione dell’insulina. E’ il test più utile per valutare la capacità residua delle cellule β del pancreas. E’ utilizzato soprattutto nel monitoraggio dell’andamento del diabete insulino-dipendente. Basse concentrazioni sieriche si riscontrano in caso di secrezione ridotta di insulina o addirittura soppresse in risposta alla somministrazione di insulina esogena; mentre valori elevati possono essere causati dall’aumento dell’attività delle cellule beta del pancreas come osservato nell‘insulinoma. Infine, poichè spesso in pazienti sottoposti a terapia con insulina vengono riscontrati anticorpi anti-insulina circolanti, che interferiscono con la determinazione dell’insulina per il diretto il controllo dell’attività residua delle cellule beta del pancreas, viene utilizzato il dosaggio del C-peptide proprio per monitorare la secrezione pancreatica di insulina.
►Clearance della creatinina – La creatinina è un prodotto del metabolismo della creatina a livello muscolare. Essendo la creatinina escreta quasi esclusivamente a livello renale, il suo valore nel sangue valuta la funzionalità renale ed una eventuale microangiopatia a livello delle arteriole renali. La clearance della creatinina è effettuata comparando le concentrazioni di creatinina nel sangue e nell’urina, per ottenere una stima calcolata della velocità di filtrazione glomerulare, nota come eGFR (Estimated Glomerular Filtration Rate). La clearance della creatinina viene calcolata moltiplicando la concentrazione di creatinina nell’urina (creatininuria) per il volume di urina prodotta nell’arco della giornata e dividendo per la concentrazione di creatinina nel sangue. Il valore finale viene espresso in mL/min. 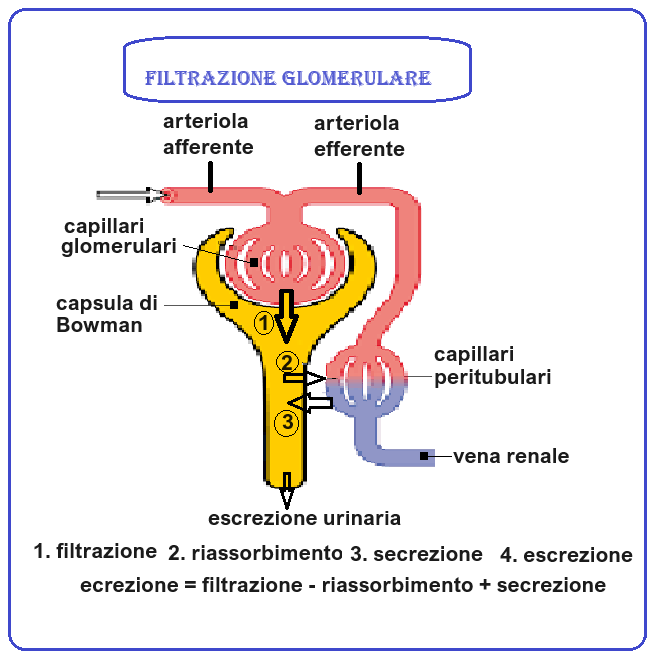
►fruttosamina, una proteina glicosilata, che consente la verifica del andamento glicemico delle ultime 2-3 settimane. A differenza dell’emoglobina glicosilata, l’esame della fruttosamina consente, non solo la verifica delle glicemia nelle ultime due settimane, ma anche l’effetto di un cambio di dieta o di terapia. I valori normali di fruttosamina sono compresi tra 2 e 2,8 mmol/l.
►Insulinemia basale (4-24 micro-unità/ml): può essere normale, aumentata o diminuita;
►Insulino-resistenza: condizione di iperinsulinemia con glicemia normale o lievemente aumentata. I meccanismi di insulino-resistenza consistono in alterazione del binding tra insulina e recettore e/o alterazioni nella trasmissione del messaggio all’interno della cellula.
►Ipercolesterolemia LDL: per aumentata sintesi a livello epatico per eccesso di Acetil-CoA
►Ipertrigliceridemia: minore metabolizzazione dei trigliceridi a causa del mancato riconoscimento di essi da parte dei recettori specifici e maggiore produzione a causa dell’aumentata lipolisi.
►Anticorpi anti-insulina
►ICA (Islat cell antibodies): anticorpi anti insule pancreatiche
►Glucagone: ormone peptidico secreto dalle cellule α delle isole di Langerhans pancreatiche. Se il livello ematico di glucosio scende sotto una soglia di circa 80 mg/dl, le cellule α cominciano a secernere glucagone. Questo si lega immediatamente ai suoi recettori presenti principalmente sugli epatociti, attivando la degradazione del glicogeno presente nelle cellule epatiche (glicogenolisi epatica) e conseguente rilascio di glucosio nel sangue. In caso di iperglicemia si riduce la secrezione di glucagone.
►ESAME URINE:
- Proteinuria, iperazotemia da microangiopatia renale
- ipercreatininuria da microangiopatia renale
- Glicosuria: in gravidanza non attendibile perchè in gravidanza sono possibili glicosurie fisiologiche da abbassamento della soglia renale per il glucosio.
- Chetonuria: ac. β-OH-butirrico, ac. aceto-acetico e acetone sono prodotti ultimi del catabolismo lipidico e proteico. L’esaltazione della lipolisi produce una maggiore quantità di Acetil-CoA a livello epatico che non viene ossidato facilmente a CO2 e H2O tramite il ciclo di Krebs (per il deficit di ac. ossalacetico consumato dai processi di neoglucogenesi). L’acetil-CoA quindi non ha altre strade che quella di condensarsi e trasformarsi in aceto-acetil-CoA e quindi ac. aceto-acetico e b-OH-Butirrico con conseguente chetonemia e chetonuria. I corpi chetonici sono sostanze acide escrete con le urine ed eliminate insieme a Na+; la perdita di cationi fa diminuire il pH plasmatico determinando la comparsa dell’acidosi metabolica.
- Microalbuminuria: presenza di albumina nelle urine in quantità modesta (20-200 mg/L) ma significativa. Nel diabete è un segno precoce di microangiopatia glomerulare ed aumento della loro permeabilità.
- Urinoculture in serie
- α-1-FP sierica materna: diminuisce proporzionalmente con l’aumento dei valori di emoglobina glicosilata (HbA1c). Nelle gravidanze con valori di HbA1c >10% e AFP diminuita c’è la tendenza a manifestare un precoce ritardo di crescita fetale (IUGR).
DIAGNOSTICA STRUMENTALE
- Esame del fondo oculare: per valutare eventuale microangiopatia a livello delle arteriole del fondo oculare
- Misurazione della pressione arteriosa
Eziopatogenesi del diabete gestazionale: (vedi file)
Nel 1º periodo (fino alla 20ª w) prevale globalmente un effetto anabolico dovuto alla aumentata produzione di ormoni steroidei (estrogeni e progesterone) e al conseguente iperinsulinismo associato ad un aumento della sensibilità periferica all’insulina; è sostanzialmente aumentata l’utilizzazione periferica del glucosio e l’immagazinamento di lipidi mentre è diminuita la neoglucogenesi.
Nella IIª parte della gravidanza, prevalentemente per l’azione dell’HPL, del glucagone e del cortisolo si verifica uno stato di insulino-resistenza. A causa di questo stato di insulino-resistenza, il fabbisogno di insulina aumenta progressivamente nella IIª parte della gravidanza di circa il 30% con picchi elevati di richiesta dopo i pasti principali. In condizioni di digiuno i valori della glicemia materna sono più bassi rispetto alla donna non gravida, mentre dopo i pasti sono più elevati. Modificazioni metaboliche nella gravida diabetica: quando la produzione endogena di insulina è insufficiente a contrastare lo stato di insulino-resistenza, si verifica l’insorgenza di diabete gestazionale. Oltre ai livelli elevati di glicemia, queste pazienti presentano elevati livelli plasmatici di trigliceridi, acidi grassi liberi e aminoacidi gluconeogenetici soprattutto in condizioni di digiuno.
 EFFETTI DELLA GRAVIDANZA SUL DIABETE: La gravidanza esercita un effetto diabetogeno notevole: A) tramite alcuni ormoni diabetogeni quali l’ACTH e l’HPL che aumentano con il progredire della gravidanza; B) consumo notevole di insulina da parte della placenta; C) ridotta sensibilità periferica all’insulina. La donna sana reagisce con una iperincrezione di insulina ciò che è invece difficile per la gestante diabetica che ha ridotte riserve di insulina. I° trimestre e puerperio: possibilità di coma ipoglicemico; La paziente diabetica in gravidanza non deve guidare per il rischio di improvvise crisi ipoglicemiche. II° e III° trimestre: è più frequente il coma diabetico. In travaglio di parto l’instabilità metabolica fa sì che la paziente possa passare con grande rapidità dall’ipoglicemia al coma diabetico e chetoacidosi con molta rapidità. Malgrado l’iperplasia, il tessuto insulare pancreatico fetale non può svolgere una funzione vicariante sul metabolismo materno perché il passaggio diaplacentare dell’insulina è molto scarso.
EFFETTI DELLA GRAVIDANZA SUL DIABETE: La gravidanza esercita un effetto diabetogeno notevole: A) tramite alcuni ormoni diabetogeni quali l’ACTH e l’HPL che aumentano con il progredire della gravidanza; B) consumo notevole di insulina da parte della placenta; C) ridotta sensibilità periferica all’insulina. La donna sana reagisce con una iperincrezione di insulina ciò che è invece difficile per la gestante diabetica che ha ridotte riserve di insulina. I° trimestre e puerperio: possibilità di coma ipoglicemico; La paziente diabetica in gravidanza non deve guidare per il rischio di improvvise crisi ipoglicemiche. II° e III° trimestre: è più frequente il coma diabetico. In travaglio di parto l’instabilità metabolica fa sì che la paziente possa passare con grande rapidità dall’ipoglicemia al coma diabetico e chetoacidosi con molta rapidità. Malgrado l’iperplasia, il tessuto insulare pancreatico fetale non può svolgere una funzione vicariante sul metabolismo materno perché il passaggio diaplacentare dell’insulina è molto scarso.
EFFETTI DEL DIABETE SULLA GRAVIDANZA:
a) Aborto, spesso ripetuto e tardivo; frequenza doppia rispetto alle gravide normali (30% vs 15%).
b) Polidramnios
c) Ipertensione arteriosa e/o riduzione della funzionalità renale su base vascolare;
f) Aumentata incidenza di placenta previa
g) Parto pretermine (da ricordare la ritardata maturazione polmonare fetale a causa dell’effetto inibitorio esercitato dall’insulina);
h) Ipocinesia in travaglio di parto
i) Sindrome delle gambe senza riposo (Restless legs syndrome, RILS): si è osservato un aumentata incidenza della RILS in pazienti diabetiche in generale ed in particolare nelle donne gravide. La stessa RILS aumenta in gravidanza a causa dei disturbi del sonno, ansia e depressione, disturbi tipici della donna gravida, che inducono insulino-resistenza ed alterazioni metaboliche (19-30). Per chi soffre di RLS andare al cinema o a teatro o ai concerti è un grande tormento come fare lunghi viaggi in auto, perché non possono sopportare di dover tenere le gambe ferme così a lungo. La diagnosi della RLS spesso si ottiene già attraverso l’anamnesi del paziente e facendo domande specifiche: se qualche membro della famiglia soffre già di questa malattia, se si è in stato di gravidanza, se sussistono malattie internistiche o neurologiche, se e quali farmaci si assumono, ecc. Anche se la diagnosi della RLS in molti casi viene fatta già in base all’anamnesi, il test nel laboratorio del sonno è spesso fondamentale. La polisonnografia (test effettuato dal “laboratorio del sonno”) è in realtà l’unico modo per diagnosticare davvero la RLS. Ciò è tanto più importante quando i sintomi non si manifestano chiaramente ma allo stesso tempo vengono segnalati disturbi del sonno.
l) ittero
ALTERAZIONI PLACENTARI:
- Aumento di spessore e di peso della placenta; invece diminuzione di peso e spessore se vi sono alterazioni vascolari. Il peso fetale è correlato ai valori della placenta. Nel tessuto placentare fetale le alterazioni vascolari non sono molto diffuse; invece sono molto frequenti nella decidua basale e a carico dei vasi del miometrio.
- Le alterazioni vascolari consistono in deposizione di materiale lipoideo, ipertrofia, ialinizzazione e degenerazione fibrinoide. Zone di necrosi placentari più o meno estese e calcificazioni. Caratteristica la coesistenza di zone ipermature e zone immature. Notevole aumento di glicogeno e fosfatasi alcalina termostabile nel citoplasma del sinciziotrofoblasto.
Il 40% delle gravide con diabete gestazionale sviluppa un diabete di tipo II dopo il parto e dopo la remissione del diabete gestazionale, anche a distanza di 5 anni. Il diabete gestazionale non controindica l’allattamento al seno.
EFFETTI DEL DIABETE SUL FETO:
- a) Embriopatie e malformazioni
- b) Morte intrauterina del feto: la causa di morte intrauterina fetale nelle gravidanze diabetiche non è ben chiaro sebbene la riduzione o l’eliminazione di questo fenomeno in gravidanze diabetiche ben controllate indichino al giorno d’oggi l’iperglicemia materna come un fattore causale importante.
- c) L’associazione fra iperglicemia materna, distress fetale e ipossia fetale nelle gravide diabetiche suggerisce come la morte intrauterina fetale sia probabilmente conseguente ad uno stato di ipossia. Le
pazienti diabetiche hanno un flusso ematico ridotto durante il 3º trimestre e questo flusso tende a diminuire ulteriormente se il controllo della glicemia non è adeguato (2-4).
- d) Ritardo precoce dello sviluppo: Il diabete si associa ad un ritardo precoce dello sviluppo che in seguito viene mascherato dalla macrosomia relativa o assoluta secondaria all’iperinsulinismo.
- e) Macrosomia fetale
- f) distocia di spalla
- g) fratture ossee, frattura delle clavicole
- h) paralisi ostetrica Nelle gravide diabetiche con nefropatia: la placenta è piccola, la produzione di steroidi è bassa, il feto è piccolo.
- Macrosomia (se non vi è vasculopatia) presente spesso anche in pazienti con buon equilibrio glicemico; la macrosomia fetale sembrerebbe correlata alI’perplasia delle isole del Langherans fetali e al peso materno pregravidico (5).
- Ipoglicemia: è molto frequente e può assumere caratteri di estrema gravità se non trattata
- Ittero: è molto frequente
- Iperinsulinemia: l’eccesso di glucosio proveniente dal distretto materno viene metabolizzato ed accumulato dal feto e induce una iperplasia del tessuto insulare del feto (le cellule β-pancreatiche sono presenti nel feto dalla 16a dettimana) e quindi iperinsulinemia. L’iperinsulinemia provoca crisi ipoglicemiche nel neonato aggravata dal fatto che ancora manca la risposta adrenalinica all’ipoglicemia e quindi non si può avere nè la inibizione della secrezione della insulina nè la mobilizzazione degli acidi grassi.
- Mortalità perinatale: aumenta con il crescere della gravità del diabete materno; è particolarmente elevata in caso di nefropatia diabetica. Sindrome da distress respiratorio (RDS) provocata quasi sempre dall’induzione di un parto prematuro in una patologia come il diabete notoriamente associata ad un ritardo della maturazione polmonare fetale. alterata tolleranza glucidica, obesità ritardo mentale.
- Malformazioni congenite: la loro incidenza (3-4 volte superiore alla popolazione non diabetica) non si è modificata di molto anche dopo l’avvento della terapia insulinica e del monitoraggio fetale. Ciò probabilmente sta a significare che l’effetto teratogeno avviene in epoca gestazionale molto precoce (attorno alla 4ª settimana) e quindi solo uno stretto controllo metabolico nelle prime fasi del concepimento o addirittura prima del concepimento potrà ridurne l’incidenza (1). Le principali malformazioni sono a carico del SNC, cuore e rene. Una conferma indiretta dell’importanza dell’equilibrio glicemico nello sviluppo embrionale è dato dalla misurazione dell’Hb glicosilata: quanto più è elevata l’Hb glicosilata tanto maggiore è il rischio di malformazioni.
- Policitemia
- Iperbilirubinemia
- Ipocalcemia
- Cardiomegalia
PROFILASSI DELLE COMPLICANZE DIABETICHE:
- Individuazione della gravida a rischio diabetico;
- Corretta terapia insulinica e alimentare
- Corretto management della gravidanza
- Modalità e momento di espletamento del parto.
Il monitoraggio glicemico e la terapia insulinica riducono il rischio di complicanze perinatali, senza aumentare la percentuale di parti cesarei (9).
Individuazione della gravida a rischio diabetico: Il miglior test di screening del diabete gestazionale è il dosaggio della glicemia plasmatica a digiuno e 60’ dopo carico orale di50 g di glucosio. Esso deve essere eseguito tra la 24ª e la 28ª settimana. Il valore-soglia deve essere posta a 135 mg/dl. Quest’esame deve essere eseguito seguendo i criteri stabiliti nel 1964 da O’ Sullivan e Mahan: la paziente viene tenuta per tre giorni a dieta libera con ingestione di almeno 150 g di carboidrati al giorno. Il test non deve essere effettuato durante situazioni di stress. Non devono essere assunte nè caffeina nè nicotina. Il mattino dell’esame si può bere acqua ma non cibi contenenti calorie. Durante l’esame la paziente dovrebbe rimanere sdraiata. Si esegue un prelievo di base (a digiuno), e subito dopo si somministrano 50 gr di glucosio sciolti in acqua da ingerire in 5’. Vengono effettuati altri 3 prelievi (dopo 30’, 60’ e 120’).

TERAPIA: l’obiettivo è tenere la glicemia sotto controllo (glicemia a digiuno <110 mg/dl e glicemia <130 mg/dl a 60′ dai pasti) mediante somministrazione di insulina, dieta ed esercizi fisici allo scopo di evitare complicazioni per la madre e per il feto.
- Terapia insulinica pre-ipo-glicemizzante: introdotta in Italia da Roversi nel 1970 con l’intento di mantenere la gravida diabetica in uno stretto equilibrio glicemico evitando l’effetto somogi (Oscillazione della glicemia, con picchi verso l’alto e/o verso il basso, causati o da un dosaggio elevato di insulina oppure da una reazione spontanea). Il management della terapia insulinica è complessa e prevede un costante monitoraggio della glicemia. Le gravide con diabete di tipo I sono ad alto rischio di ipoglicemia.
- Insulina pronta: è somministrata tre volte al dì alla dose di 5 Unità inferiore a quella che produce ipoglicemia (l’ipoglicemia è evidenziata dall’insorgere di sudorazione). Eventualmente aggiungere insulina retard a sera.
- Sconsigliato in gravidanza l’uso di ipoglicemizzanti orali per il rischio teratogeno e per la possibilità di insorgenza di ipoglicemia nel neonato.
- Metformina (Metforal® cpr 500 mg, 850 mg, Glucophage® cpr 500 mg, 850 mg, 1000 mg unidie): attualmente è approvata dalla Food and Drug Administration per il trattamento del diabete di tipo 2 (9). Nel foglietto illustrativo si avverte che l’uso della metformina è controindicato in gravidanza; tuttavia sia in Canada sia negli Stati Uniti è in crescita l’uso off-label di tale farmaco nel trattamento dell’infertilità causata da PCOS. La metformina facilita il concepimento nelle donne affette da oligomenorrea e PCOS (10,11). Recenti studi hanno suggerito che l’uso di metformina durante la gravidanza riduce l’elevata incidenza di aborti spontanei in donne PCOS (30-50%) e di diabete gestazionale (31% delle donne non trattate contro il 3% delle donne trattate) (12-14).
- Vildagliptin: potenzia la secrezione di insulina da parte delle cellule beta del pancreas e inibisce la secrezione di glucagone da parte delle cellule alfa. In associazione con Metformina è commercializzato con il nome di Eucreas® (Eucreas cpr 50 mg/1000 mg; 50 mg/850 mg). Il vildagliptin è un inibitore potente e selettivo della DPP-4 (dipeptidil peptidasi-4). Il DPP-4 è l’enzima responsabile della degradazione delle incretine GLP-1 (peptide-1 glucagone-simile) e GIP (polipeptide insulinotropico glucosio-dipendente), ormoni intestinali secreti dopo i pasti e che stimolano le cellule beta del pancreas a produrre insulina. L’azione delle incretine è correlata con i livelli di glicemia infatti, maggiori sono i livelli glicemici, più l’incretina stimola la secrezione di insulina, mentre se i livelli di glicemia sono nella norma, l’azione delle incretine è minore (38-43). E’ opportuno non somministrare in gravidanza e allattamento.
- Libramed® bustine: complesso macromolecolare che costituisce un gel aderente alle pareti intestinali in modo da rallentare e contrastare l’assorbimento dei carboidrati. Assunto, disciolto in un bicchiere di acqua, poco prima dei pasti principali consente di evitare e moderare i picchi glicemici post-prandiali.
- Caffè, azione antidiabete: la dose massima di caffeina ammissibile durante la gravidanza, secondo l’American College of Obstetricians and Gynecologist, è di 200 mg al giorno (2 tazzine di caffè espresso). Dosi superiori avrebbero un effetto negativo sulla gravidanza aumentando le percentuali di aborto spontaneo a causa della presenza di caffeina che produce ipertensione acuta (molto modesta nei bevitori abituali), e di due diteroenoidi alcoolici (cafestolo e kahweol) che inducono iprcolesterolemia, Le concentrazioni di questi diteroenoidi alcoolici dipendono soprattutto dalla modalità di preparazione del caffè. Il caffè bollito (ad esempio il caffè turco) ha elevate concentrazioni di cafestolo e cafeolo poichè essi vengono estratti dai chicchi di caffè nel contatto prolungato con l’acqua. . Secondo molti altri studi, il caffè avrebbe un effetto anticancerogeno su prostata e fegato ed inoltre contrasterebbe l’insorgenza di diabete tipo 2 (25%) e diabete gestazionale. Il caffè, mediante i suoi composti fenolici, ed in particolare dell’ac. clorogenico, è in grado di inibire gli enzimi intestinali deputati alla digestione dei carboidrati. Questa azione, esercitata anche dal decaffeinato, determina un rallentamento nell’assorbimento del glucosio ed attenua così il picco glicemico che si osserva dopo il consumo di un pasto, contribuendo alla riduzione del rischio di diabete di tipo 2. L’ipotesi è stata confermata dai dati sperimentali, che, però sono stati ottenuti in vitro e vanno confermati da uno studio in vivo condotto sull’uomo. In conclusione è opportuno limitarsi a 1-2 tazzine di caffè in gravidanza e non oltre le tre tazzine al di fuori della gravidanza (17).
- dieta: La dieta prevede pasti piccoli e frequenti (3 piccoli pasti e 2 spuntini) allo scopo di evitare i picchi iperglicemici. La dieta deve essere normocalorica o solo moderatamente ipocalorica, iperproteica (20%), 30% lipidi e carboidrati in percentuale non inferiore al 50%. I carboidrati devono essere forniti forniti prevalentemente da verdure (tutte le verdure verdi in foglie, asparagi, sedani, cetrioli). In una gravida non a rischio si consiglia una dieta di 2.000-2.200 Kcal. Nelle p/ti a rischio di diabete gestazionale si prescrive una dieta da 1.600 Kcal nella prima parte della gravidanza e 1.800 Kcal nell’ultima parte.
Gli idrati di carbonio sono comunque necessari al fegato per metabolizzare i grassi; in mancanza di carboidrati vi sarà acidosi con gravi conseguenze per il feto. E’ essenziale introdurre molta fibra vegetale grazie alla verdura e ai legumi debitamente conteggiati nella dieta.
Sono vietati: datteri, castagne, frutta sciroppata, fichi secchi, prugne secche, uva, ciliege. Sono vietate: bevande alcoliche, vino (a parte la quantità concessa in dieta), birra, liquori, superalcolici, amari, aperitivi, digestivi. Sono vietate: bevande zuccherate tipo: coca cola, aranciata, limonata, chinotto, bitter, spuma, acqua tonica, acqua brillante e bibite con dicitura senza zucchero, tè zuccherati. Sono vietati: zucchero, miele , budini, marmellata , cioccolato , dolci e pasticceria in genere, gelatina di frutta, gelati, succhi di frutta dolcificati, caramelle, cioccolatini, sciroppi, conserva di frutta.
Gli alimenti con dicitura “senza zucchero” sono proibiti in quanto contengono glucidi e carboidrati, sia sotto forma di amidi, sia zuccheri come sorbitolo, galattosio, ecc. E’ inoltre molto importante fare pasti ben equilibrati fra loro.
Camminare è l’esercizio più semplice da fare in gravidanza e fa diminuire del 5-10% il rischio  di diabete gestazionale nelle donne obese. Anche la ginnastica pre-parto contribuisce alla profilassi antidiabetica.
di diabete gestazionale nelle donne obese. Anche la ginnastica pre-parto contribuisce alla profilassi antidiabetica.
I carboidrati possono essere classificati come:
- Zuccheri semplici ad assorbimento molto rapido (glucosio, fruttosio, galattosio);
- Zuccheri semplici ad assorbimento rapido (saccarosio, lattosio, maltosio);
- Zuccheri complessi o polisaccaridi ad assorbimento lento (amido e glicogeno).
Con il diabete meglio la pasta degli zuccheri. Una volta ingerito un alimento contenente degli zuccheri, siano essi semplici o complessi, per essere assorbiti dall’intestino devono essere demoliti fino alla struttura più semplice del glucosio; questa molecola passa come tale nel sangue, in cui è possibile misurarne la quantità . Essendo la velocità di assorbimento inversamente proporzionale alla complessità dello zucchero, è importante escludere dalla dieta gli zuccheri semplici che comportano bruschi e rapidi aumenti di glicemia (alto indice glicemico); al contrario andranno privilegiati gli alimenti contenenti carboidrati complessi. In genere gli alimenti con basso indice glicemico sono uova, formaggi, pesce, carne e ortaggi, mentre quelli che presentano questo parametro alto sono soprattutto riso, patate, pane bianco, zucchero, dolci e miele. Pasta, riso e pane di tipo integrale contengono molte più fibre, che ostacolano la produzione di insulina e l’aumento della glicemia. Inoltre i cibi integrali favoriscono il transito intestinale, sgonfiando la pancia, e regalano un maggiore senso di sazietà. Occorre ridurre l’ingestione di NaCl sostituendolo con spezie e peperoncino rosso.
La cottura – Quando si parla di indice glicemico il tipo di cottura è fondamentale. La pasta cotta al dente si accompagna ad un assorbimento più lento dell’amido e quindi si abbassa l’indice glicemico. Nel pane tostato è neutralizzata l’azione dell’amido. Le patate vanno consumate bollite e sempre fredde per abbattete il loro indice glicemico
Il condimento – Condire sempre i cibi con olio extravergine d’oliva, optare per le spezie per insaporire. Associate la pasta a verdure e legumi, il riso al pesce e alle patate.
L’esercizio fisico moderato come brevi passeggiate effettuate regolarmente fa diminuire dal 10% al 5% il rischio di insorgenza di diabete gestazionale nelle pazienti obese.
Corretto management della gravidanza: Non stress test (NST) eseguito 2 volte a settimana dalla 35ª settimana in poi.
Scelta del tempo e della modalità del parto: Poiché una delle più gravi conseguenze della fetopatia diabetica è la morte intrauterina improvvisa del feto è fondamentale un monitoraggio accurato per una scelta del tempo e delle modalità di espletamento del parto che risulterà sempre da una somma di considerazioni che prevedono maturità e benessere del feto e condizioni di salute della madre. Se le condizioni locali della gestante sono favorevoli, il diabete è ben compensato, non vi è sofferenza fetale nè macrosomia, la via vaginale rappresenta la modalità ideale di espletamento del parto. Nel caso in cui non si verifichi un travaglio di parto spontaneo, di solito si preferisce procedere ad induzione non prima della 40-41ª w. Monitoraggio biofisico continuo durante il travaglio. Controllo della glicemia durante il travaglio ed eventuale terapia endovenosa con insulina pronta in caso di glicemia >120 mg/dl. Sembra che la necessità di ricorrere al Taglio Cesareo sia da attribuire all’aumento ponderale materno (6). In caso di taglio cesareo somministrare insulina rapida endovena 1 UI/3 gr di glucosio.
CRISI IPOGLICEMICHE – L’ipoglicemia viene solitamente definita come la concentrazione di glucosio plasmatico inferiore a 50-55 mg/dl. Il 45% delle donne con diabete di tipo 1 e il 19% delle donne con diabete di tipo 2 presentano episodi di ipoglicemia severa in gravidanza. L’ipoglicemia è più frequente nelle gravide diabetiche con anamnesi di crisi ipoglicemiche pregravidiche, non corretto management della terapia insulinica, inadeguato apporto di carboidrati, eccesso di attività fisica. Oltre a questi fattori è stata evidenziata un’alterata risposta controregolatoria ormonale all’ipoglicemia in gravidanza riferibile a ipersensibilità all’insulina in gravidanza, aumento progressivo della concentrazione di insulina durante la gravidanza con picco al 3° trimestre, ridotta risposta di adrenalina e glucagone all’ipoglicemia rispetto alle donne non gravide e non diabetiche. Il meccanismo non è chiaro ma sembra che tale effetto inibitorio sia da attribuire agli ormoni placentari.
Gli effetti degli episodi ipoglicemici sulla madre sono quelli osservati fuori dalla gravidanza (tremore, sudorazione profonda, nausea, vomito, fame, stanchezza, sonnolenza, lipotimia, cefalea, confusione mentale, progressivo deterioramento cognitivo fino al coma, convulsioni, morte). Sul feto gli effetti teratogeni e quelli sulla frequenza cardiaca fetale (tachicardia/bradicardia) sono oggetto di pareri discordanti.
Terapia e prevenzione delle crisi ipoglicemiche – Tipicamente l’ipoglicemia viene trattata assumendo immediatamente cibi e bevande ad alto indice glicemico come dolci, caramelle e succo d’arancia. Le nuove formulazioni di analoghi dell’insulina disponibili ad azione sia rapida sia basale hanno fortemente ridotto il rischio di ipoglicemie. La possibilità di utilizzare, anche in gravidanza, un sistema di monitoraggio continuo della glicemia (Continuous Glucose Monitoring, CGM) che, tramite un sensore sottocutaneo, registra le escursioni glicemiche interstiziali durante tutto il giorno ad intervalli di 5 minuti (288 misurazioni/die) e li trasmette wireless, ad un ricevitore applicato sulla cute della paziente. Il CGM 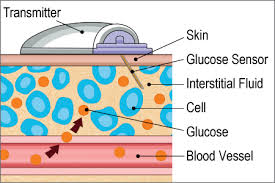 permette di conoscere esattamente ed in tempo reale l’insorgenza, la frequenza e durata degli episodi ipoglicemici e di ricorrere prontamente ai presidi terapeutici prima dell’insorgenza di gravi alterazioni sistemiche.
permette di conoscere esattamente ed in tempo reale l’insorgenza, la frequenza e durata degli episodi ipoglicemici e di ricorrere prontamente ai presidi terapeutici prima dell’insorgenza di gravi alterazioni sistemiche.
Il CGM può essere utilizzato in modalità real time, in modalità flash (il ricevitore viene attivato quando la paziente lo avvicina al sensore) o retrospettivo. In quest’ultimo caso si ha un quadro pressochè completo dell’andamento glicemico giornaliero e le variazioni in rapporto a esercizio fisico, pasti, assunzione di farmaci, malattie.
La rappresentazione della curva glicemica consente di approntare adeguate misure preventive con diminuzione della variabilità glicemica e della HbA1c. Il sistema CGM è provvisto di meccanismi di allarme per ipo- ed iperglicemia (utilissimi soprattutto nelle ore notturne), frecce di tendenza e trasmissione dei dati in remoto (nigtscout system) (35-37).
La determina G08900 del 03/08/2016 stabilisce le indicazioni alla prescrivibilità del CGM in unione al CSII da parte del SSN italiano. Sono in fase sperimentale avanzata apparecchi non invasivi per CGM.
MANAGEMENT DEL DIABETE DOPO IL PARTO: L’allattamento al seno deve essere favorito. 6 settimane dopo il parto sottoporre la paziente a curva da carico di glucosio con 75 gr di glucosio per os al fine di identificare ogni forma di diabete latente.
CONCLUSIONE: Le donne sottoposte a controllo intensivo ed eventuale insulinoterapia hanno partorito in genere bambini di peso inferiore e di età gestazionale inferiore, e l’induzione del travaglio è stata significativamente più comune (39% contro 29%). Non si è registrata invece alcuna differenza nella frequenza del parto cesareo. 3 mesi dopo il parto l’8% delle donne nel gruppo trattato presentava sintomi di depressione, contro il 17% del gruppo non trattato.
References:
- Schwartz ML, Ray WN, Lubarsky SL: The diagnosis and classification of gestational diabetes mellitus: is it time to change our tune? .Am J Obstet Gynecol. 1999 Jun; 180(6 Pt 1):1560-71.
- Vanderijst JF, Debiève F, Doucet F, Emonts P, Haumont S, Hubinont C, Kirkpatrick C, Philips JC, Pintiaux A, Rousseau P, et al.: [Screening strategy and diagnostic criteria for gestational diabetes. Proposals of the GGOLFB]. Rev Med Brux. 2012 Mar-Apr; 33(2):97-104.
- P. Lonero Baldassarra, A. Kardashi, P. Greco, A. Vimercati, N. Pansini, G. Loverro, L. Selvaggi: “Fattori di rischio nel diabete gestazionale”. Giorn It. Ostet. Ginec. N.3/1997.
- Boerschmann H, Pflüger M, Henneberger L, et al. Prevalence and Predictors of overweight and insulin resistance in offspring of mothers with gestational diabetes mellitus. Diabetes Care. 2010 Apr 30.
- Nylund L., Lunell N. O., Lewander R. et al.: Uteroplacental blood flow in diabetic pregnancy. Measurements with indium-113m and a computer-linked gamma camera. Am. J. Obstetr. Gynecol. 144:298-302,1982.
- Nordalander E. , Hanson U., Persson B. : Factors Influencing Neonatal Morbility In Gestational Diabetic Pregnancy . Br. J. Obst. Gyn. , 96,671,19989.
- Witter F. R., Caulfield L. E., Stoltzfus R. J.: Influence of maternal anthropometric status and birth weight on the risk of cesarean delivery. Obst. Gynec., 85, 947,1995.
- PAULA A. RADON, MD, MICHAEL J. MCMAHON, MD, MPH and WILLIAM R. MEYER, MD: “Impaired Glucose Tolerance in Pregnant Women With Polycystic Ovary Syndrome” Obstetrics & Gynecology 1999;94:194-197.
- CA Crowther et al.: “Effect of treatment of gestational diabetes mellitus on pregnancy outcomes”. N Engl J Med 2005;352:2477-2486
- Barbieri RL. Metformin for the treatment of polycystic ovary syndrome. Obstet Gynecol 2003; 101: 785-793.
- Danaif A. Insulin resistance and the polycystic ovary syndrome: mechanism and implications for pathogenesis. Endocr Rev 1997; 8: 774-800.
- United States Food and Drug Administration. Metformin product monograph. Washington, DC: United States Food and Drug Administration; 2000. Available
- Ben Haroush A, et al. Insulin resistance and metformin in polycystic ovary syndrome. Eur J Obstet Gynecol Reprod Biol 2004; 115: 125-133.
- McCarthy EA, et al. Metformin in obstetric and gynecologic practice: a review. Obstet Gynecol Surv 2004; 59: 118-127.
- Glueck CJ, et al. Continuing metformin throughout pregnancy in women with polycystic ovary syndrome appears to safely reduce first-trimester spontaneous abortion: a pilot study. Fertil Steril 2001; 75: 46-52.
- Glueck CJ, et al. Metformin therapy throughout pregnancy reduces the development of gestational diabetes in women with polycystic ovary syndrome. Fertil Steril 2002; 77: 520-525.
- Briggs GG, et al. Drugs in pregnancy and lactation. Philadelphia, Pa: Lippincott, Williams and Wilkins; 2002.
- Pereira, MA e coll. Coffee consumption and risk of type 2 diabetes mellitus. A 11-year prospective study. Arch.Int.Med. 2006: 166, 1311
- Gamaldo CE, Earley CJ. Restless legs syndrome. A clinical update. Chest 2006; 130: 1596-604.
- Phillips B, Young T, Finn L, Asher K, Hening WA, Purvis C. Epidemiology of restless legs symptoms in adults. Arch Intern Med 2000; 160: 2137-41.
- Berger K, Luedemann J, Trenkwalder C, John U, Kessler C. Sex and the risk of restless legs syndrome in the general population. Arch Intern Med 2004;164: 196-202.
- Allen RP, Picchietti D, Hening WA, Trenkwalder C,Walters AS, Montplaisir J. Restless legs syndrome:
diagnostic criteria, special considerations and epidemiology; a report from the Restless legs syndrome
diagnosis and epidemiology Workshop at the National Institutes of Health. Sleep Med 2003; 4:101-19. - Banerji NK, Hurwitz IJ. Restless legs syndrome, with particular reference to its occurrence after gastric surgery. BMJ 1970; 4: 774-5.
- Ohayon MM, Roth T. Prevalence of restless legs syndrome and periodic limb movement disorder in
the general population. J Psychosom Res 2002; 53:547-54. - Schlesinger I, Erikh I, Avizohar O, Sprecher E, Yarnitsky D. Cardiovascular risk factors in restless legs syndrome. Movement Disorders 2009; 24: 1587-92.
- Keckeis M, Lattova Z, Maurovich-Horvat E, et al. Impaired glucose tolerance in sleep disorders. PLoS
One 2010; 5: e9444. - Bosco D, Plastino M, Fava A, et al. Role of the oral glucose tolerance test (OGTT) in the idiopathic restless legs syndrome. J Neurol Sci 2009; 287: 60-3.
- Lopes LA, Lins CMM, Adeodato VG, et al. Restless legs syndrome and quality of sleep in type 2 diabetes. Diabetes Care 2005; 28: 2633-6.
- Merlino G, Fratticci L, Valente M, et al. Association of restless legs syndrome in type 2 diabetes: A case control study. Sleep 2007; 30: 866-71.
- Skomro RP, Ludwig S, Salamon E, Kryger MH. Sleep complaints and restless legs syndrome in adult
type 2 diabetics. Sleep Med 2001; 2: 417-22. - Hod M1, Kapur A2, Mcintyre HD3; FIGO Working Group on Hyperglycemia in Pregnancy and the FIGO Pregnancy and Prevention of early NCD Committee . Laboratory standardization is important in the diagnosis of gestational diabetes. Am J Obstet Gynecol. 2019 Feb 23.
- Lee B, Lee JS, Lee YW, Jang MA, Song J, Kim JH, Lee WG, Min WK, Lee J, Lee YK: Effect of the Standardization of Diagnostic Tests on the Prevalence of Diabetes Mellitus and Impaired Fasting Glucose. J Korean Med Sci. 2018 Mar 5; 33(10):e81. Epub 2018 Mar 5.
- Validation of administrative and clinical case definitions for gestational diabetes mellitus against laboratory results. Bowker SL, Savu A, Donovan LE, Johnson JA, Kaul P.Diabet Med. 2017 Jun; 34(6):781-785. Epub 2016 Nov 16.
- Poolsup N Systematic review and meta-analysis of the effectiveness of continuous glucose monitoring (CGM) on glucose control in diabetes Diabetes Diabetol Metabol Syndr 2013 Jul 23;5:39
- El-Laboudi Ahmed H et al «Measures of Glycemic Variability in Type 1 Diabetes and the Effect of Real-Time Continuous Glucose Monitoring” Diabetes Technology & Therapeutics. December 2016, 18(12): 806-812
- Feig DS et al “Continuous glucose monitoring in pregnant women with type 1 diabetes (CONCEPTT):
a multicentre international randomised controlled trial” Lancet. 2017 Sep 14. pii: S0140-6736(17) - Thomas L. Lemke, David A. Williams, Victoria F. Roche, S. William Zito, Foye’s Principi di Chimica Farmaceutica, a cura di F. Dall’Acqua, VI edizione italiana, Piccin, pp. 945-946,
-
Keating GM Vildagliptin: a review of its use in type 2 diabetes mellitus. Drugs 2010 Nov 12;70(16):2089-112.
- Vildagliptin: a review of its use in the management of type 2 diabetes mellitus.
Croxtall JD, Keam SJ.Drugs. 2008; 68(16):2387-409.
- Vildagliptin: clinical trials programme in monotherapy and combination therapy for type 2 diabetes.
Rosenstock J, Fitchet M.Int J Clin Pract Suppl. 2008 Mar; (159):15-23.
- Effects of vildagliptin on glucose control in patients with type 2 diabetes inadequately controlled with a sulphonylurea. Garber AJ, Foley JE, Banerji MA, Ebeling P, Gudbjörnsdottir S, Camisasca RP, Couturier A, Baron MA.Diabetes Obes Metab. 2008 Nov; 10(11):1047-56. Epub 2008 Feb 18.
- A comparison of efficacy and safety of vildagliptin and gliclazide in combination with metformin in patients with Type 2 diabetes inadequately controlled with metformin alone: a 52-week, randomized study. Filozof C, Gautier JF.Diabet Med. 2010 Mar; 27(3):318-26.
Queste pagine fanno parte del sito fertilitycenter.it in internet da marzo 2011. I testi, le tabelle, i disegni e le immagini pubblicati in queste pagine sono coperte da copyright ma a disposizione di tutti per copia e riproduzione purchè venga citata la fonte con Link al sito www.fertilitycenter.it. Ringrazio i lettori per la loro cortese attenzione e li prego di voler comunicare le loro osservazioni e consigli su eventuali errori o esposizioni incomplete.
Enzo Volpicelli.





1 commento
Howdy. Very nice site!! Guy .. Excellent .. Wonderful .. I will bookmark your web site and take the feeds also…I am glad to locate so much useful information here in the post. Thank you for sharing.