Ultimo aggiornamento 21:12:43 2020-01-28
La trombosi venosa profonda (TVP) è una flebotrombosi di una vena profonda, quasi sempre degli arti inferiori e particolarmente dell’arto inferiore sinistro (1). In genere inizia a livello delle valvole venose del polpaccio dove il sangue è relativamente povero di ossigeno.
Le trombosi della v. porta, della vena renale e della v. epatica (S. di Budd-Chiari) vengono definite e trattate come patologie autonome.
La trombosi venosa profonda (TVP) e l’embolia polmonare (EP) costituiscono due delle principali cause di mortalità materna in ostetricia (2). Il parto ed il puerperio rappresentano, infatti, condizioni a rischio per via delle modificazioni emodinamiche ed endocrine materne (3).
Fequenza: lo 0,74% del numero totale dei parti è complicato, nel post-partum, da una TVP. Nel 90% dei casi la TVP si manifesta al 1° giorno di puerperio e soprattutto (75%) in caso di taglio cesareo (3),. Vi sono però notevoli discordanze in letteratura per quanto riguarda la frequenza relativa degli eventi tromboembolici nel corso di gravidanza e puerperio (4). Non c’è dubbio, comunque, che la gravidanza e il puerperio siano fattori predisponenti l’insorgenza di una TVP (3,18). Infatti il rischio di tromboembolismo venoso associato con la gravidanza è stato stimato essere cinque volte superiore a quello di una donna non gravida di pari età (4). L’aumentato rischio può essere attribuibile a diversi fattori:
- la stasi venosa, conseguente a:
- compressione sulle vena cava inferiore e sulle vene iliache pelviche da parte dell’utero gravido, ancor più frequente nelle gravidanze gemellari (5) e nella macrosomia fetale. La compressione venosa, la stasi venosa e una ipercoagulabilità costituiscono la “triade di Virchow”.
- Iperplasia dell’a. iliaca comune destra e relativa compressione sulla vena omonima (11).
- prolungata permanenza a letto di gravide a rischio;
2. le modificazioni in senso procoagulanteche si manifestano nel corso della gravidanza e che coinvolgono i fattori della coagulazione e della fibrinolisi. Le alterazioni della coagulazione comprendono:
- l’aumento dei livelli plasmatici dei fattori III, VII, e X che si verifica a partire dal quarto mese di gestazione (6), associato ad un aumento della formazione di fibrina (7);
- la riduzione dei livelli plasmatici di proteina S, e l’assenza di modificazioni dei livelli plasmatici della proteina C (8);
- l’inibizione dell’attività fibrinolitica che si riscontra particolarmente nel III° trimestre di gravidanza (9).
3. Infarti placentari e distacco di placenta
5. Aborto spontaneo o procurato
6. il parto: Il parto per via vaginale e soprattutto il taglio cesareo inducono una situazione di rischio tromboembolico simile a quello associato a qualsiasi altro intervento chirurgico addomino-pelvico (12). Dopo taglio cesareo, la probabilità di una complicanza trombotica è aumentata fino a 10 volte rispetto al parto per via vaginale (13). Ciò è principalmente da imputare a embolizzazione trofoblastica.
7. il puerperio: nel puerperio l’incidenza di TVP subisce un incremento per quelle donne costrette a letto per lunghi periodi (15).
8. malattie procoagulatorie preesistenti (policitemia vera, Sindrome di Leiden, etc.)
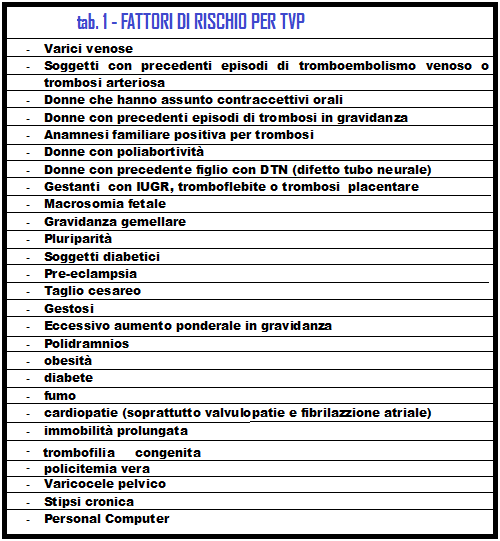
Il rischio d’insorgenza di una TVP aumenta in quelle pazienti in cui alla gravidanza si associano altri fattori predisponenti (tab. 1) fra i quali sono preminenti la presenza di vene varicose, la trombofilia ereditaria e il varicocele pelvico.
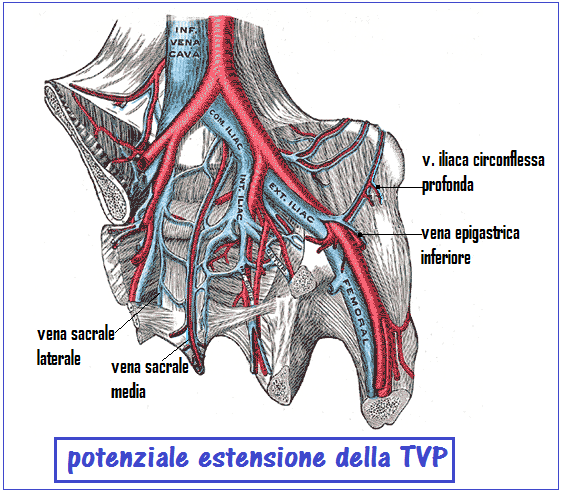
Complicanze: la TVP può estendersi facilmente a distretti venosi unguinale e pelvici ma il pericolo principale è quello del distacco di emboli che circolando nel flusso sanguigno potrebbero giungere fino ai polmoni determinando una embolia polmonare.
Clinica della TVP:
i sintomi sono correlabili all’evento trombotico e/o embolico:
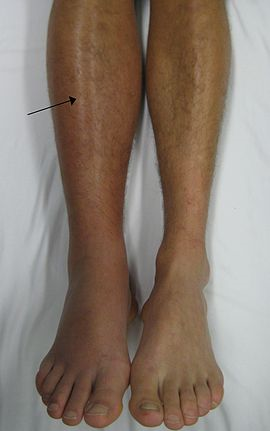
- dolore, gonfiore e cute calda in un tratto localizzato degli arti inferiori
- a livello dell’arto inferiore,
- senso di pesantezza agli arti inferiori,
- crampi,
- prurito,
- edema: Un lieve edema degli arti inferiori è normale durante la gravidanza. Ma un improvviso edema importante associato a dolori al polpaccio o all’intero arto inferiore sono sospetti per una TVP.
DIAGNOSTICA:
- PDF: Prodotti di Degradazione del Fibrinogeno che derivano dalla trasformazione della fibrina insolubile, propria del coagulo e derivata dal fibrinogeno ad opera della trombina e stabilizzata dal fattore XIIIa, in prodotti di degradazione ad opera dell’enzima proteolitico denominato plasmina. In caso di TVP i valori sierici dei PDF sono superiori alla norma (v.n. <10 mg/ml). Fra di essi il più noto ed importante è il D-dimero.
- D-dimeri: i d-dimeri (due frammenti legati tra loro da un legame covalente) sono i frammenti più piccoli derivati dalla disgregazione della fibrina. Il D-dimero esprime un’attivazione della fibrinolisi. I valori del D-dimero (v.n. <250 ng/ml) aumentano fisiologicamente in gravidanza, in puerperioe nel post-intervento; aumenta nelle donne fumatrici, nei traumatismi e nelle patologie epatiche e renali. Si tratta quindi di un esame a bassa specificità ma che in presenza di risultati negativi esclude con una certezza quasi assoluta la diagnosi di tromboembolismo venoso. Per questo sua elevata specificità, il ruolo diagnostico del D-dimero è proprio quello di escludere, in presenza di valori bassi, la trombosi venosa profonda e l’embolia polmonare.
Potrebbe interessarti: http://www.my-personaltrainer.it/salute/d-dimero.html - PT e PTT sono monitorizzati in tutte le pazienti, soprattutto per controllare l’efficacia della terapia antitrombotica con Calciparina.
- Fattore plasmatico VIII
dopo l’insorgenza della sintomatologia, si possono eseguire:
- · Eco-color Doppler flussimetria
- · pletismografia degli arti inferiori.
- · TC con mezzo di contrasto è utile per fare la diagnosi di trombosi delle vene iliache, delle vene ovariche e di altre vene pelviche.
- RX del torace
- scintigrafia polmonare perfusionale
- fleboscintigrafia ileo-cavale prima del posizionamento del filtro cavale.
- Emogasanalisi su sangue arterioso, che può mettere in evidenza una eventuale ipossiemia arteriosa associata ad alcalosi respiratoria.
Se si sospetta un’embolia polmonare, si può effettuare senza rischi una scintigrafia polmonare ventilatoria/perfusionale, perché la dose di radiazioni a cui è esposto il feto è <0,2 Gy. Difetti di perfusione si rilevano nel 20% delle pazienti nel post-partum, probabilmente a causa di una embolizzazione trofoblastica durante il parto. Se la diagnosi di EP non è certa, è necessario eseguire l’angiografia polmonare. Il trattamento acuto, accanto all’eparina EV, prevede la lisi enzimatica con l’urochinasi o con l’attivatore tissutale del plasminogeno. Le embolie ricorrenti, che si verificano nonostante una adeguata terapia anticoagulante, richiedono un trattamento chirurgico che prevede il posizionamento percutaneo di un filtro cavale, come l’ombrello di Greenfield, subito al di sotto dei vasi renali.
TERAPIA:
Nelle pazienti che presentano fattori di rischio, è applicata
- una elasto-compressione all’arto o agli arti inferiori il giorno del parto. La terapia elasto-compressiva permette di ottenere buoni risultati, ma non tutte le pazienti la gradiscono e, soprattutto, vi può essere la ricomparsa dei sintomi qualora il trattamento venga sospeso (32).
- profilassi farmacologica in tutte le pazienti sottoposte a taglio cesareo.
- Subito dopo l’espletamento del parto, in tutti i casi, è necessaria
– Calciparina® fl s.c. 5.000 e 12.500 UI (7.500 UI x 2) o altre eparine a basso peso molecolare (LMWH) come Clexane® fiale s.c. 2.000 UI, 4.000 UI (enoxaparina sodica); Fraxiparina®, Seleparina® (Nadropina calcica) fiale preriempite da 0.3, 0,4, 0.6, 0.8, 1 ml; ogni ml equivale a 9500 UI anti Xa. La somministrazione è effettuata per via sottocutanea 1 volta al dì per la profilassi e 2 volte al dì per la terapia mentre l’eparina non frazionata (UFH) richiede 3-4 somministrazioni al dì. Recentemente però sono stati sollevati dubbi sulla reale efficacia terapeutica delle (LMWH) nel trattamento e prevenzione delle tromboflebiti e TVP e relative complicanze come IUGR, aborto, distacco di placenta, gestosi ipertensiva (39,40).
– Warfarin (Coumadin® cpr 5 mg x 2/die) antagonista competitivo della vitamina K, monitorizzando il tasso di attività protrombinica (PT e PTT).
– farmaci antinfiammatori non steroidei,
– enzimi proteolitici (33).
- In alcune pazienti è necessario posizionare un Tempofilter Cavale da rimuovere generalmente dopo circa un mese, mentre in alcune pazienti è necessario un posizionamento definitivo.
Complicanze della terapia trombolitica: sindrome post-trombotica
PROFILASSI:
un’attenta e tempestiva profilassi, sia per la possibilità di prevenire molte forme di patologia venosa, ma soprattutto per ridurre, se non annullare del tutto, l’incidenza della complicanza più temibile: l’embolia polmonare (30). Negli USA, la tromboembolia è la causa principale della mortalità materna dovuta a complicanze mediche, essendo diventata negli ultimi 10 anni più frequente delle emorragie, delle infezioni e della malattia ipertensiva. L’aumento di incidenza è correlato in parte all’aumento della frequenza dei parti cesarei e in parte al miglioramento della diagnosi di trombosi.
Profilassi farmacologica con eparina a basso P.M. (2000 UI x 2) in tutte le pazienti sottoposte a taglio cesareo. La profilassi con eparinato di calcio, dopo la risoluzione del fatto acuto, va proseguita anche nel puerperio, in quanto,la condizione di elevato rischio tromboembolico permane per almeno 6 settimane dopo il parto, anche se il primitivo episodio appare clinicamente risolto (34).
Se l’episodio si è verificato in una precedente gravidanza, alcuni consigliano di attuare la profilassi antitrombotica con eparinato di calcio già all’inizio della nuova gravidanza, o meglio, già 3-4 settimane prima del concepimento. La profilassi farmacologica deve poi essere continuata in puerperio, prima con l’eparinato di calcio, e poi proseguendo con dicumarolici per via orale (35).
Arixtra (Fondaparinux) è un inibitore selettivo del Fattore Xa ed il primo farmaco di una nuova classe farmacologica, indicato nella prevenzione della trombosi venosa profonda. Arixtra, agendo in modo selettivo sul Fattore Xa, interrompe in modo precoce la formazione dei coaguli. Arixtra è somministrata per via sottocutanea al dosaggio di 2,5 mg una sola volta al giorno, 6-8 ore dopo l’operazione chirurgica. Arixtra è controindicato nei pazienti con funzione renale gravemente alterata o nei pazienti con peso corporeo inferiore a 50 kg, perché questi pazienti sono a più elevato rischio di sanguinamento, così come i pazienti d’età superiore ai 75 anni.
Tuttavia il provvedimento preventivo più importante nell’immediato puerperio consiste nel mobilizzare precocemente la paziente, ed evitare tutte quelle condizioni in grado di favorire la stasi venosa agli arti inferiori. Si consiglierà, pertanto, alla paziente di alzarsi dal letto non appena possibile, evitare di mantenere a lungo la stazione eretta, o la posizione seduta, senza muoversi (37).
La terapia con warfarin durante la gravidanza è stata associata alla morte e all’insorgenza di anomalie fetali e non ci sono prove che il destrano a basso peso molecolare e i FANS siano sicuri; quindi, l’anticoagulante di scelta è l’eparina a basso peso molecolare. A causa delle sue dimensioni molecolari, l’eparina non attraversa la placenta. Nelle pazienti con una trombosi venosa profonda (TVP) o con un’embolia polmonare (EP) confermate, la terapia con eparina va instituita immediatamente.
Consigli per prevenire la TVP:
- sdraiarsi durante la giornata con le gambe in alto;
- dormire con i piedi rialzati, mettendo un cuscino sotto il materasso;
- camminare con scarpe comode e leggermente rialzate, a suola morbida e chiuse dietro (non le ciabatte);
- possibilmente nuotare o fare ginnastica in acqua.
Bibliografia
- Letsky E.A.: Peripartum prophilaxy of thromboembolism. Baillieres Clin. Obstet. Gynecol. Sep; 11(3): 523 43, 1997.
- Woodhams B.J., Candotti G., Shaw R. et al.: Changes in coagulation and fibrinolysis during pregnancy: evidence of activation of coagulation preceding spontaneous abortion. Thromb. Res.; 55:99-107, 1989.
- Pavel J.L., et al.: Hypercoagulable states as on evolving risk for spontaneous venous and arterial thrombosis. J. Am. Coll. Surg., 178,266-70, 1994.
- National Institutes of Health Consensus Development Conference: Prevention of venous Thrombosis and pulmonary embolism. JAMA; 256:744-9, 1986.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma; cap. XXX: pp 860-64,1990 a.
- Colman R.W., Cook JJ., Niewiarowski S.: Mechanism of Platelet Aggregation. In Colman R.W., Hirsh J., Marder V.J., Saliman E.W. Haemostasis and Thrombosis: basic principles and clinical practice. Third edition J.B. Lippincott Company, Philadelplia. pp 508-23, 1994.
- Weiner C.P., Kwaan H., Hauck W.W., et al.: Fibrin generation in normal Pregnancy. Obstet. Gynecol. 64:46-48, 1984.
- Faught W., Gamer P., Jones G. et al.: Changes in protein C and protein S in normal Pregnancy. Am J. Obstet. Gynecol, 172:147-50, 1995.
- Bremme K., Ostlund E., Almquist I et al.: Enhanced Thrombin generation and fibrinolitic activity in normal pregnancy and puerperium. Obstet. Gynecol. 80:132-137, 1992.
- Ginsberg J.S., Brili-Edwards P., Burrows R.F. et al.: Venous Thrombosis During Pregnancy: Leg and trimester of presentation. Thromb. Haemost.; 67: 519-20, 1992.
- Cockett F.B., Thomas M.L., Negus D.: Iliac vein compression: its relation to ileofemoral thrombosis and the post-thrombotic syndrome. Br. Med. J.; 2: 14, 1967.
- Berquist D., Hedner U.: Pregnancy and venous thromboembolis. Acta Obste. Gynecol. Scand; 62; 449-63, 1983.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma; cap. XXX: pp 860-64,1990 a.
- Nicolaides A.N. e Irving D.: Clinical Factors and the risk of deep vein thrombosis. In Thromboembolism: aetiology, advanced in prevention and management. Nicolaides (ed). Lancaster, EngIand, MPT Press, 1975.
- Nicolaides A.N. e Irving D.: Clinical factors and the risk of deep vein thrombosis. In Thromboembolism: aetiology, adva-nced in prevention and management. Nicolaides (ed).Lancaster,England, MPT Press, 1975.
- Gerbasi F.R., Bottoms S., Farag A. et al.: Increased intravascular coagulation associated with pregnancy. Obstet. Gynecol.; 75: 385-9, 1990.
- Berquist D., Hedner U.: Pregnancy and venous thromboembolis. Acta Obste. Gynecol. Scand; 62; 449-63, 1983.
- Kruithof E.K., Tran-Thang C., Gudinchet A. et al.: Fibrinolysis in pregnancy: a study of plasminogen activator inhibtors. Blood; 69:460-6, 1987.
- Hilesmaa V.: Occurrence and anticoagulant treatment of thrombo-embolis in gravidas, parturients and gynecologic patients: a study of 678 cases treated in the Women’s Clinic of theUniversity ofHelsinki in 1953-57. Acta Obstet. Gynecol. Scand.; 39: Suppl. 2: 5-12, 1960.
- Drill V.A., Calhonn D.W.: Oral Contraceptives and thromboembolic disease. JAMA; 206:77, 1968.
- Rutherford S., Montoro M., McGehee W., et al.: Thromboembolic disease associated with pregnancy: an 11 years review. Am J. Obstet. Gynecol; 164: Suppl. 286. Abstract, 1991.
- Pini M., Scoditti U., Caliumi F., et al.: Risk of venous thromboembolism and stroke associated with oral contraceptives. Role of congenital Thrombophilias. Rec. Progr. Med.; 87: 331-7, 1996.
- Kierkegaard A.: Incidence and diagnosis of DVT associated with pregnancy. Acta Obste. Gynecol. Scand; 62: 239, 1983.
- Speiser W., Maller R., Koppensteiner R., et al.: D-dimer and TaT measurement in patients whit DVT: Utility in diagnosis and judgement of anticoagulant treatment effectiveness. Thromb. Haemost: 64, 196, 1990.
- Bounameaux H., Schneider P.A., Reber G., De Moerloose P.: Measurement of plasma D-dimer for diagnosis of DVT. Am J. Clin. Pathol. 1989: 91,82.
- Bounarneaux H., Schneider PA., Reber G., De Moerloose P.: Measurement of plasma D-dimer for diagnosis of DVT. Am. J. Clin. Pathol. 1989:91,82.
- Charman C.S., Arhtar N., Campbell S., Miles K., O’Connor J., Mitchell V.E.: The use of D-dimer assay by enzime Immunoassay and latex agglutination Techniques in the diagnosis of DVT. Clin. Lab. Haernat. 1990:12,37,
- Nieuwenhuinzen W.: New strategies in the determination of fibrin and fibrin(ogen) derivates by monoclonal antibodies. Blut; 57(5)285-291, 1998.
- Bounameaux H., Cirafici P., De Moerloose P., et al.: Measurement of D-dimer in plasma as diagnostic aid in suspected pulmonary embolism. Lancet; 337: 196-200, 1991.
- Letsky E.A.: Peripartum propholaxy of thromboembolism. Baillieres. Clin. Obstet. Gynaecol. Sep; 11(3): 523-43, 1997.
- Letsky E.A.: Peripartum prophilaxy of thromboembolism. Baillieres. Clin. Obstet. Gynaecol. Sep; 11(3): 52343, 1997.
- Nicoladies A.N., et al.: Value of ambulatory pressure in the assessment of venous insufficiency. Vascular diagnosis and therapy; 3,41-50, 1981.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma; cap. XXX. pp 860-64,1990 a.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma; cap XXX pp 860-64,1990 a.
- Letsky E.A.: Peripartum Prophilaxy of thromboembolism. Baillieres. Clin. Obstet. Gynaecol. Sep; 11(3): 523-43, 1997.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma; cap. XXX: pp 860-64,1990 a.
- Pescetto G., De Cecco L., Pecorari D., Ragni N.: Manuale di Ginecologia e Ostetricia. Società Editoriale Universo, Roma, cap. XXX: pp 860-64,1990 a.
- Rowbotham B.J., Carrol P., Whitaker A.N., et al.: Measurement of cross linked fibrin derivates: use in the diagnosis of venous thrombosis. Thromb.Haemostas. 57,59, 1987.
- Rodger MA, Hague WM, Kingdom J, Kahn SR, et al, for the TIPPS Investigators. Antepartum dalteparin versus no antepartum dalteparin for the prevention of pregnancy complications in pregnant women with thrombophilia (TIPPS): a multinational open-label randomised trial. The Lancet. 25 July 2014. DOI: 10.1016/S0140-6736(14)60793-5. Available at: http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(14)60793-5/abstract
- Ottawa Hospital Research Group. Common blood thinner for pregnant women proven ineffective: Lancet study. July 24, 2014. Available at: http://www.ohri.ca/newsroom/newsstory.asp?ID=500