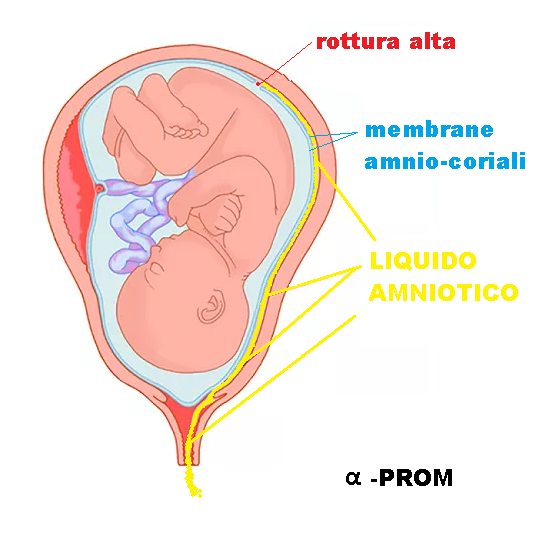
Membrane amnio-coriali: Al di là della zona placentare dove come corion frondosum concorre a costituire la placenta, la membrana derivante del corion laeve è trasparente, resistente, fibrosa. Aderisce mediamente con un sottile strato di connettivo all’amnios. Situata all’interno del corion, la membrana amniotica è costituita da un unico strato di cellule epiteliali cubiche di origine ectodermica. Sotto all’epitelio troviamo la membrana basale, lo strato compatto, lo strato fibroblastico, lo strato spongioso, lo starto reticolare e quindi una membrana basale che divide-separa l’amnios dal corion.
Si definisce prematura la rottura delle membrane (corion e amnios) che avviene prima del travaglio. Precoce se avviene a travaglio iniziato.
A sua volta la rottura prematura si distingue in rottura prematura delle membrane a termine (premature rupture of membranes, PROM), rottura prematura pre-termine delle membrane (pPROM) prima della 37ª settimana, early pPROM se la rottura avviene prima delle 23 settimane e rottura parziale o incompleta delle membrane detta anche rottura alta (a-PROM).
Frequenza: PROM: 10%; pPROM: 2%.
Etiologia PROM:
1) Ipertensione della cavità ovulare in toto (contrazioni uterine, polidramnios, gravidanza gemellare, microsomia fetale).
2) Ipertensione della parte inferiore della cavità ovulare (viziature pelviche, presentazioni anomale, tumori previ).
3) Diminuita elasticità delle membrane (endometriti, placenta previa).
4) Traumi diretti o indiretti, urti accidentali, sforzi, eccesso di esplorazioni vaginali (nelle pazienti a rischio PROM si raccomanda di procedere all’esplorazione vaginale esclusivamente con l’ausilio di uno speculum sterile!).
5) Amniocentesi (1%)
6) Infezioni-infiammazioni: si verifica:
- liberazione diretta di proteinasi da parte dei microrganismi;
- aumento della produzione di collagenasi ed in particolare delle metalloproteinasi (MMP) per azione delle endotossine batteriche,
- depressione degli inibitori tissutali delle MMP (TIMP) da parte delle interleuchine (IL-8 e TNF) prodotte dai neutrofili e monociti richiamati dalla reazione flogistica.
7) Alterazioni genetiche: nella Sindrome di d’Ehlers-Danlos si osserva un assottigliamento dello spessore delle membrane.
8) Diminuita concentrazione sierica di Cu, Zn e vitamina C (2).
9) Tabagismo: fa raddoppiare i casi di RPM-pRPM inibendo la fagocitosi batterica da parte dei macrofagi e quindi favorendo le infezioni-infiammazioni-iperproduzione di leuchine.
FISIOPATOLOGIA PROM:
I fattori etiologici comportano un’iperproduzione non bilanciata di PGE2, PGF2-α, IL-8, Relaxina e aumento della apoptosi con frammentazione del DNA e RNA in corrispondenza del punto di rottura (1).
Inoltre, la fitta rete di fibre collagene che normalmente stabilizza il sacco amniotico,viene dissolta in caso di PROM e lo spessore del sacco amniotico è ridotto. La misurazione USG dello spessore delle membrane può fornire una valutazione prognostica del rischio di PROM: (v. n. 1± 0.7 mm) (10-14).
SINTOMATOLOGIA PROM:
fuoriuscita improvvisa, con o senza concomitanti contrazioni uterine, di liquido amniotico in quantità variabile, che per il suo riformarsi, continua a scolare e che aumenta con i movimenti della donna o se, con il riscontro vaginale, si sposta in alto la parete distale delle membrane.
DIAGNOSI:
Non presenta grosse difficoltà. Il metodo più semplice ed economico è la visione diretta del LA che scola dal canale cervicale.
La diagnosi differenziale è da porsi con incontinenza urinaria, abbondante leucorrea e l’idrorrea (o idroematorrea deciduale):
1) L’incontinenza urinaria si esclude inserendo un catetere in vescica e con questa manovra cessa lo scolo di liquido oppure determinando il pH in quanto l’urina ha un pH acido mentre il LA ha un pH basico.
2) La profusa leucorrea è in genere clinicamente riconoscibile, altrimenti è sufficiente un esame microscopico del liquido raccolto; in esso si osserveranno cellule epitliali pavimentose, batteri.
3) Idrorrea deciduale – Più complessa è la differenziazione con la idrorrea deciduale (scolo di liquido formatosi tra la decidua parietale e riflessa in genere per una deciduite). La idrorrea deciduale si verifica in genere tra la 14a e la 28a settimana di gestazione, è più scarsa, non aumenta con i movimenti della madre e del feto e inamida la biancheria. Una diagnosi più precisa può aversi con l’esame microscopico (presenza di lanugine fetale, di cellule fetali, di globuli di grasso (colorazione Sudan III), se si tratta di liquido amniotico).
PROGNOSI PROM:
La prognosi materna è in genere buona. La prognosi fetale è due volte più infausta del normale, sia per la prematurità che per l’inquinamento della cavità amniotica, con conseguenze settiche a carico dell’apparato respiratorio fetale, della cute, dell’apparato neurologico anche a distanza di anni (5). Dopo le 32 settimane, in assenza di complicanze materno-fetale, la terapia migliore è principalmente quella di attesa sotto copertura antibiotica e tocolitica. Fra 24-26 w la prognosi fetale è severa sia in caso di parto immediato che di prolungamento della gravidanza ed è fondamentale il counseling con la coppia. Sotto le 23 w si impone il giudizio clinico. 23 settimane è la soglia per l’ipoplasia polmonare (6). Dopo le 34 w la prognosi è favorevole (6).
COMPLICAZIONI PROM:
1) insorgenza prematura del travaglio: a seconda dell’epoca gestazionale, può essere abortivo, partoprematuro, parto precoce. Il periodo di latenza fra rottura bassa delle membrane ed insorgenza del travaglio è di solito di poche ore; diventa spesso molto più lungo quando la rottura si è verificata in un periodo molto lontano dal termine della gravidanza, specie se la paziente è nullipara.
2) corionamnionite: la più importante complicazione quando l’intervallo tra rottura ed inizio del travaglio si prolunga oltre le 48 h. Ad essa può seguire anche una setticemia anche attuando una terapia antibiotica a largo spettro e a dosi piene.
- Infezioni neonatali: intervengono nel 15% dei casi; è più frequente nelle p-RPM; sono precedute o concomitanti a corionamnionite.
- Morte fetale: la percentuale di morte fetale intrauterina in pPROM fra 16 e 25 w è di 4-22% mentre a 30-36 w è del 0-2% (6).
- addossamento delle pareti uterine al prodotto del concepimento:
- disturbi di circolazione placentare che si manifestano con alterazioni del BCF (tachicardia iniziale che può trasformarsi in bradicardia in caso di sofferenza fetale) .
- Compressione degli arti fetali con alterazioni del tipo artrogriposi (piede torto) e displasia dell’anca legate all’immobilismo degli arti.
- ipoplasia polmonare: è una patologia caratterizzata da riduzione del volume e peso dei polmoni a causa di una diminuzione del numero degli alveoli polmonari. Ha una frequenza del 50% nei feti <1.000 gr o malformati (8). In gravide con pPROM prima della 26a w con periodo di latenza di 1-5 settimane è del 16-50% e la mortalità fetale per tale patologia raggiunge l’87.5% mentre dopo la 26° w l’incidenza della IP cala precipitosamente (3,6). L’IP può essre primitiva con una frequenza di 0.1% o secondaria a condizioni che causano compressione del torace: PROM, oligoamnios, idrope fetale, ernia diaframmatica, S. di Prune Belly che determina una megavescica per ostruzione uretrale (8). La IP può essere diagnosticata in utero mediante USG con la misurazione della circonferenza toracica mediante la formula D1xD2x1.57; i calipers sono posti in posizione esterno-esterno in una sezione trasversa del torace che includa le 4 camere cardiache.
- Deformazione facciale
- Ritardo di crescita
- il prolasso del funicolo.
- difficoltà al secondamento.
- Malattia da membrane ialine (MMH): è una delle complicazioni più importanti della prematurità.
- Leucomalacia periventricolare (PVL): è la principale lesione neurologica riscontrata nella RPM. Si tratta di necrosi della sostanza bianca agli angoli esterni dei due ventricoli laterali. Le tossine liberate dai batteri sono responsabili della flogosi e ischemia e quindi necrosi tissutale (4). La PVL è il più importante predittore di paralisi cerebrale.
- Emorragia intraventricolare: insieme alla PVL costituisce le lesioni cerebrali caratteristiche della PROM (7). L’emorrgia intraventricolare produce distensione dei ventricoli laterali e distruzione conseguente della parete ependimale e, nei casi più gravi, interessare il parenchima cerebrale a causa della compressione dei capillari ventricolari e conseguente ischemia della sostanza bianca cerebrale; se l’ischemia non è prontamente corretta i radicali liberi prodotti dall’ischemia aggrediscono gli oligodendrociti che vanno in necrosi per danno citotossico. Inoltre le citochine che fuoriescono dai capillari danneggiati aggrediscono direttamente gli oligodendrociti (7).
- Enterocolite necrotizzante
- Trombosi da meconio: in caso di rottura delle membrane amnio-coriali molto tempo prima del parto (pPROM e early pPROM) ed emissione di meconio, possono verificarsi un’ampia degenerazione dell’epitelio ed una necrosi dei vasi fetali con trombosi intravascolari.
Complicazioni della PROM alta:
nella α-PROM le gravidanza può proseguire indisturbata anche per parecchie settimane; talvolta si assiste alla chiusura spontanea della breccia. Dato che la soluzione di continuo è distante dal canale cervicale, il rischio di infezioni è molto ridotto.
MANAGEMENT della PROM:
- TAGLIO CESAREO – Taglio cesareo appena la maturazione polmonare ed il peso sono soddisfacenti: molti AA considerano più importante il rischio di infezioni materne e fetali che quello di prematurità fetale. Da 34 settimane in poi è preferibile praticare un cesareo profilattico. Anche perchè spesso non si riesce a prevenire la corionamnionite anche attuando una terapia antibiotica a largo spettro e a dosi piene.
Altri AA. instaurano terapia ritardante il parto quando l’evento patologico si verifica in un periodo compreso fra la 32ª e la 34ª w, quando cioè procrastinare il parto anche di pochi giorni può essere decisivo per la sopravvivenza fetale.
C’è comunque da ricordare che non è possibile attenersi ad una rigida schematizzazione, ma che la nostra decisione non può prescindere da altre considerazioni (parità della paziente, condizioni materne, eventuale presenza di un attrezzato centro neonatale con TIN, ecc.) e la decisione finale spetta ad un giudizio clinico. Speroff definisce giudizio clinico una decisione da prendersi quando non si hanno tutti gli elementi necessari per prendere una decisione. La gestione di una pPRM sotto le 23 w è un classico caso per applicare il giudizio clinico non essendoci studi clinici randomizzati (6).
- Riposo assoluto a letto in ambiente tranquillo.
- Somministrazione di farmaci tocolitici:
- a) b-bloccanti[1]: Isossisuprina, Bufenina, Orciprenalina, Ritodrina, ecc.
La dose di attacco è rappresentata da infusione endovenosa a goccia lenta di uno dei suddetti farmaci con aggiunta di progesterone ad alte dosi. In seguito, in assenza di attività contrattile, si potrà passare alla somministrazione per os dei farmaci tocolitici. In caso di terapia prolungata con beta-mimetici è opportuno controllare gli elettroliti in quanto i farmaci tocolitici determinano deplezione di potassio. La tachicardia materna, oltre che fetale, è un evento fisiologico in corso di terapia tocolitica ma può nascondere o mimare uno stato infettivo.
- b) Calcio-antagonisti[2]: hanno un’efficacia minore ma minori effetti collaterali
- Generosa somministrazione di antibiotici a largo spettro, sia per via generale (endovena e orale insieme) che endovaginale per evitare il più possibile le infezioni endoamniotiche. I farmaci da utilizzare preferibilmente sono le ampicilline a dosi di 2-3 gr/die e, per le prime 48 ore, eritromicina e.v./os per 5 giorni. In caso di persistenza di iperpiressia (streptococco b-emolitico) occorre associare l’ac. clavulonico che però fa aumentare le percentuali di enterocolite necrotizzante. La terapia antibiotica deve proseguire anche in puerperio per ovvie ragioni profilattiche.
- Tampone cervicale per la ricerca di germi gram+ e gram – tra cui Chlamydia trachomatis e Neisseria gonorrhoeae e tampone rettale per Streptococcus agalactiae (Streptococco del gruppo B). Il tampone va mantenuto nell’ampolla rettale per circa 30 secondi, continuando a muoverlo e a ruotarlo contro le pareti dell’intestino.
- Somministrazione di betametasone[3] per favorire la maturazione del Surfactant e ridurre i rischi di membrane ialine, frequenti proprio nei prematuri, nelle 24 ore precedenti il parto. La terapia cortisonica può essere utilizzata anche in periodo gestazionale più precoce ed essere poi ripetuta nel periodo immediamente pre-parto: diversi AA. hanno riferito circa la sopravvivenza di feti di 28 settimane sottoposti previamente a terapia con Betametasone. Circa l’uso del betametasone non tutti gli autori sono d’accordo in caso di membrane rotte. Molti anzi, vedono in questo caso una controindicazione assoluta, come in caso di diabete e gestosi, in quanto ritengono che il rischio di fenomeni infettivi, favoriti dalla rottura delle membrane e dalla depressione dei meccanismi immunitari indotta dal cortisone, è tanto alto da non essere preferibile a quello di membrane ialine. Oltre a questo fanno anche un’altra considerazione, e cioè che la rottura stessa del sacco è di per sè un potente stimolo induttivo sulla maturazione del Surfactant, per cui, dopo circa 72 ore dalla rottura del sacco non dovrebbero più esserci problemi di membrane ialine. Questi stessi autori hanno ultimamente introdotto l’uso della Teofillina[4], sembra con risultati incoraggianti, al posto del Desametasone, alla dose di 250 mg x 2/die in vena ripetibile.
- Limitare al massimo i riscontri vaginali, facilitano le infezioni e l’induzione del parto.
- Riscontro della temperatura corporea almeno ogni 6 ore ed alla prima deviazione termica procedere subito all’espletamento del parto, se è il caso, anche mediante taglio cesareo.
- Vitamina K[5] e Fenobarbital (?): per la prevenzione delle emorragie intracraniche.
- Amnioinfusione: Consiste nell’introduzione di una soluzione salina sterile in cavità amniotica tramite un ago ecoguidato. Viene utilizzata nelle rotture premature di membrane e nell’oligoanidramnios in cui la riduzione parziale o totale di liquido amniotico favorirebbe l’ipoplasia polmonare fetale e anomalie scheletriche fetali.
L’amnioinfusione consente, tra l’altro terapie intramniotiche specifiche con antibiotici in caso di rischio di corionamniotite o con somministrazione di tiroxina per ridurre il rischio di immaturità polmonare e quindi di malattia delle membrane ialine neonatale. Consente inoltre di effettuare esami culturali su piccole quantità di liquido amniotico (6). La tecnica è gravata da possibili complicanze come distacco di placenta e corionamnioniti. Sembra avere efficacia solo nelle pazienti che riescono a mantenere parte del liquido almeno per 48 ore (6). L’applicazione dell’amniopatch potrebbe estendere l’uso di amnioinfusione anche a queste ultime pazienti.
- Patch (tappo) di concentrato piastrinico materno autologo (circa 50×109 piastrine in 20-30 ml) prodotto per aferesi e crioprecipitato contenente fibrinogeno e trombina (circa 700 mg di fibrinogeno/ml) iniettati in cavità amniotica. La conoscenza del sito di rottura non è necessaria per l’amniopatch, poiché le piastrine sembrano capaci di individuare il punto di rottura per chemiotassi e sigillarlo (16-22).
- Cerchiaggio cervicale + amniopatch + amnioinfusione
TERAPIA pPROM
Prima della 24a settimana:
- riposo a letto rigoroso,
- antibiotici,
- niente tocolitici né cortisonici
- “trasfert in uterus” del neonato presso un centro neonatale di III° livello.
Tra la 24a e 26a settimana:
- riposo a letto rigoroso,
- cortisone,
- antibiotico terapia che copra anche lo streptococco b-emolitico
- transfert presso un centro neonatale di III° livello.
BIBLIOGRAFIA:
- Wang KC, Lee WL, Wang PH. Early and late preterm premature rupture of membranes. J Chin Med Assoc. 2017 Oct;80(10):613-614.
- Sand Strass JF: “Premature rupture of the fetal membranes”. N Engl J Med 1998;338:663-670.
- French JI and McGregor JA: “The pathobiology of premature rupture of membranes”. Semin Perinatol 1996;20:344-368.
- Rotschil A, Ling EW, Puterman LM, Farquharson D: “Neonatal outcome after prolonged preterm rupture of the membranes”. Am J Obstetr Gynecol 1990;162:46-52.
- Zupan Vet al: “Periventricular leukomalacia: risk factors revisited”. Dev Med Child Neurol 1996;38:1061-1067.
- Spinillo A et al: “Eoidemiological correlates of preterm premature rupture of membranes”. Int J Gynaecol Obstet 1994;47:7-15.
- Caruso A., Scavo M. Noia G e De Santis M: “C’è ancora un razionale per il trattamento della pPROM precocissima?”. Atti SOc. It Ginec. Ostetr. 2003; Relazioni; CIC edit Roma; pagg. 290-297.
- Arpino C., Poveromo D., D’Argenzio L., Colicchio A. et Curatolo P.: “pPROM ed esiti neurologici neonatali”. Atti SOc. It Ginec. Ostetr. 2003; Relazioni; CIC edit Roma; pagg. 912-914.
- Pirillo P et Pirillo D.: “L’ipoplasia polmonare”. Atti Soc. It Ginec. Ostetr. 2003; Relazioni; CIC edit Roma; pagg 470-480.
- Vanessa Nunes, Jennifer Cross, John E. Speich, Danielle R. Morgan, Jerome F. Strauss and Ronald M. Ramus, Fetal membrane imaging and the prediction of preterm birth: a systematic review, current issues, and future directions, BMC Pregnancy and Childbirth, 10.1186/s12884-016-1176-5, 16, 1, (2016).
- Derman Başaran, Özgür Özyüncü, Özgür Kara, Nihal Şahin, Mert Turğal and Lütfü S. Önderoğlu, Ultrasonographic measurement of amniochorionic membrane in asymptomatic pregnant women is not a useful tool for preterm birth prediction, Journal of Obstetrics and Gynaecology Research, 40, 1, (62-66), (2013).
- Judy Slome Cohain, The less studied effects of Amniotomy, The Journal of Maternal-Fetal & Neonatal Medicine, 26, 17, (1687-1690), (2013).
- Jerome F. Strauss,, Extracellular Matrix Dynamics and Fetal Membrane Rupture, Reproductive Sciences,
- Fernando Arias, Antonio R. Gonzalez-Ruiz and Robert L. Jacobson, Recent advances in the pathophysiology and management of preterm premature rupture of the fetal membranes, Current Opinion in Obstetrics and Gynaecology,
-
P. Frigo, Ch. Lang, M. Sator, R. Ulrich, P. Husslein: Membrane thickness and PROM—high‐frequency ultrasound measurements. Prenatal Diagnosis 1998 Volume18, Issue 4, Pages 333-337
-
S. Sipurzynski‐Budraß, S. Macher, M. Haeusler, G. Lanzer: Successful treatment of premature rupture of membranes after genetic amniocentesis by intra‐amniotic injection of platelets and cryoprecipitate (amniopatch): a case report. Vox Sanguinis 2006;1,1:88-90
-
Contino B, Armellino F, Brokaj L, Patroncini S.: Amniopatch, a repairing technique for premature rupture of amniotic membranes in second trimester.. Acta Biomed. 2004;75 Suppl 1:27-30.
-
Sipurzynski-Budrass S, Macher S, Haeusler M, Lanzer G.: Successful treatment of premature rupture of membranes after genetic amniocentesis by intra-amniotic injection of platelets and cryoprecipitate (amniopatch): a case report. Vox Sang. 2006 Jul;91(1):88-90.
-
Sipurzynski-Budrass S, Macher S, Haeusler M, Lanzer G. Successful treatment of premature rupture of membranes after genetic amniocentesis by intra-amniotic injection of platelets and cryoprecipitate (amniopatch): a case report. Vox Sang. 2006 Jul;91(1):88-90.
-
Quintero RA, Morales WJ, Allen M, Bornick PW, Arroyo J, LeParc G. Treatment of iatrogenic previable premature rupture of membranes with intra-amniotic injection of platelets and cryoprecipitate (amniopatch): preliminary experience. Am J Obstet Gynecol. 1999 Sep; 181(3):744-9.
-
[Amniotic fluid leakage and premature rupture of membranes after amniocentesis. A review of the literature]. Abboud P, Zejli A, Mansour G, Monnoyer Y, Houareau LG, Bart H, Bock S.J Gynecol Obstet Biol Reprod (Paris). 2000 Dec; 29(8):741-745
-
Amniopatch for iatrogenic rupture of the fetal membranes. Deprest J, Emonds MP, Richter J, DeKoninck P, Van Mieghem T, Van Schoubroeck D, Devlieger R, De Catte L, Lewi L.Prenat Diagn. 2011 Jul; 31(7):661-6. Epub 2011 Jun 8.
- [1] Inderal (propranololo) cpr 40 mg; Tenormin (atenololo) cpr 100 mg
- [2] Adalat (Nifedipina) cpr 10 mg; Adalat A-R cpr sublinguali 20 mg
- Iperten (Manidipina) cpr 20 mg
- Isoptin (Verapamil) conf 40 e 80 mg; fiale 5 mg ev flebo
- [3] Celestone Cronodose fl im/sc: 2 fl i.m./12 h. x 2 giorni (Betametasone 6 mg); Bentelan fl 1.5 e 4 mg im/ev; cpr efferv 0.5 mg
- [4] Teoplus cpr 300 mg
- [5] Konakion cf masticabili 10 mg; fiale im 10 mg
- Gardenale cpr 50 e 100 mg; fiale 100 mg im; Luminale cpr 100 mg;