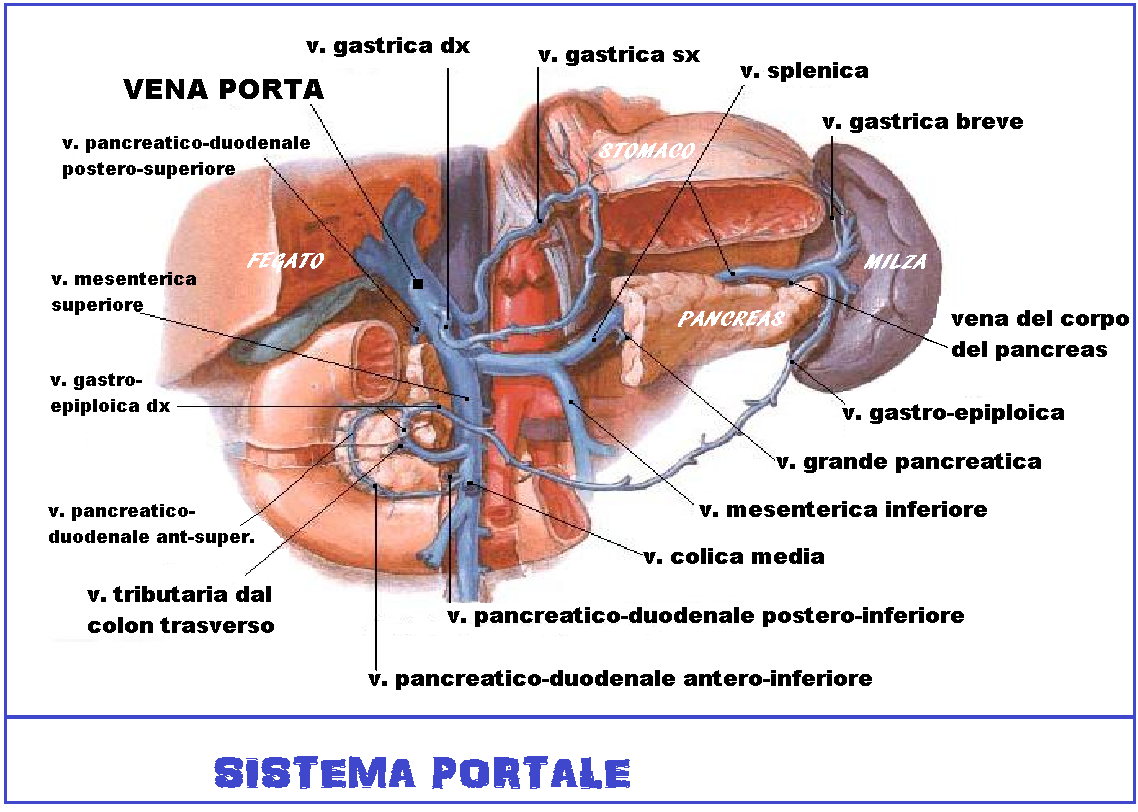
La gravidanza in pazienti con ipertensione portale è rara, ma molto preoccupante per il clinico. Anche se gli effetti di ipertensione portale durante la gravidanza non sono stati completamente chiariti, vi è un aumento evidente della morbilità, soprattutto associata a cirrosi, che giustifica la classificazione di la gravidanza a rischio e richiede una gestione da parte di un team multidisciplinare. La prevenzione e il trattamento di emorragia gastrointestinale è molto simile a quella dei pazienti non gravide. Indagine e gestione dell’ipertensione portale prima e all’inizio della gravidanza può ridurre il rischio di morte fetale, IUGR, parto prematuro e mortalità materna, che sono quasi sempre connessi ad emorragia esofago-gastro-intestinale. Da considerare anche i rischi collegati alla varicosità degli arti inferiori ed esofagea e relativi rischi tromboembolici.
In generale è da preferire il parto vaginale riservando il taglio cesareo a precise esigenze di tipo strettamente ostetrico (1-4).
Le pazienti affette da ipertensione portale (IP) sia da cirrosi che non cirrotica -non-cirrhotic portal hypertension (NCPH) – vedono peggiorare la loro patologia durante la gravidanza a causa dell’incremento del volume plasmatico, del flusso ematico e delle resistenza vascolari venose del  distretto inferiore. Quest’ultima aumenta a causa della compressione, correlata all’epoca di gravidanza, dell’utero gravido sulla vena cava inferiore (5-8).
distretto inferiore. Quest’ultima aumenta a causa della compressione, correlata all’epoca di gravidanza, dell’utero gravido sulla vena cava inferiore (5-8).
Complicanze materne dell’IP in gravidanza sono:
- insufficienza epatica acuta – comporta una morbilità del 75% e una mortalità materna e fetale del 70% entro 48 ore.
- varici arti inferiori ed esofagee: i sistemi venosi degli aa. inferiori ed esofageo costituiscono i principali circoli collaterali della vena porta e quindi in essi aumenta la pressione e si dilatano in caso di ipertensione portale (23.24).
- emorragie digestive, esofagee in particolare, sono presenti nell’8% delle gravide in cui la diagnosi di IP era stata effettuata prima della gravidanza e nel 40-70% delle gravide con IP diagnosticata per la prima volta durante la gravidanza. La maggior parte delle rotture delle varici esofagee avviene durante il III° trimestre. La rottura delle varici esofagee durante la gravidanza comporta un alto rischio di aborto (24%) e morte fetale (33.3%). Per tale motivo si raccomanda la scleroterapia endoscopica (EGDs) nelle pazienti che intendono affrontare una gravidanza (9-12).
Terapia:
- Sonde esofagee (sonda di Sengstaken-Blakemore, di Linton-Nachlas)
- Scleroterapia endoscopica pre-gravidica o in gravidanza
- Bendaggio profilattico arti inferiori
- propanololo: buoni risultati ma è gravato da complicanze fetali come IUGR, bradicardia fetale, ipoglicemia
- Terlipressina (Glipressina 1 mg fl ev 5 ml, H) vasopressore che si inietta in dose di 2 fl ev in bolo lento ogni 4-6 ore fino a scomparsa dell’emorragia e fino ad un massimo di 24 ore). Può essere utilizzata anche 30-60 minuti prima dell’intervento sclerosante a scopo profilattico per limitare emorragie e favorire l’intervento. Comporta aumentato rischio di insufficienza placentare e distacco placentare (26-31).
-
Introduzione dell’ago di Colapinto nella vena porta
TIPS (Transjugular intrahepatic portosystemic shunt) – procedura di radiologia interventistica che consiste nella creazione di un canale artificiale all’interno del fegato per stabilire una comunicazione tra la vena porta e la vena epatica allo scopo di ottenere una diminuzione della pressione venosa intra- e sovraepatica. Metodo d’elezione per il trattamento dell’ipertensione portale refrattaria alla terapia medica, in sostituzione dello shunt chirurgico. In gravidanza trova indicazione solo in casi gravi e di estrema urgenza come la sindrome epato-renale (14-17). La procedura dura circa 70 minuti e generalmente, ma non obbligatoriamente, è eseguita in anestesia generale. Tecnica TIPS: la vena giugulare costituisce la porta di ingresso di un cateterino vascolare guidato sotto scopia fluoroscopica successivamente nella vena cava superiore, v.cava inferiore e vena epatica. A questo punto si inietta CO2 per individuare la vena porta. Quindi un ago speciale
viene fatto avanzare attraverso il parenchima epatico per collegare la vena epatica alla vena grande portale, vicino al centro del fegato. Il canale per lo shunt viene creato successivamente gonfiando un palloncino per angioplastica all’interno del fegato lungo il tratto creato dall’ago. Lo shunt è completato inserendo uno stent-graft per mantenere pervio il canale (18-22). La pz. è dimessa il giorno dopo l’intervento. Controlli USG sono efettuati dopo l’intervento e settimanalmente per 2-3 mesi (32-41). Rischi e complicanze della TIPS:- Danni vascolari e parenchimali
- Febrre
- Encefalopatia epatica
- Infezioni
- Emorragie
- Gordon a. et al: PORTAL HYPERTENSION IN PREGNANCY. BJOG 1963:70,6:1056–1059
- d’Alteroche L et al: Portal hypertension and pregnancy. Gastroenterologie Clinique et Biologique [2008, 32(5 Pt 1):541-546]
- Yung-Sheng Cheng: Pregnancy in liver cirrhosis and/or portal hypertension American Journal of Obstetrics and Gynecology Volume 128, Issue 7, 1 August 1977, Pages 812-822
- Michelle A. Russell, Sabrina D. Craig: Cirrhosis and portal hypertension in pregnancy Seminars in Perinatology Volume 22, Issue 2, April 1998, Pages 156–165
- Gordon A.G. et al.: PORTAL HYPERTENSION IN PREGNANCY. BJOG 1963;70,6:1056-1059
- N. Aggarwal et al: Non-cirrhotic portal hypertension in pregnancy I J Gynec Obstet 2001;72,1:1-7
- Murali Subbaiah, Sunesh Kumar, Kallol Kumar Roy, Jai Bhagwan Sharma, Neeta Singh, Extrahepatic portal-vein obstruction in pregnancy, Taiwanese Journal of Obstetrics and Gynecology, 2015, 54, 4, 394CrossRef
- Z. Jabiry-Zieniewicz, F. A. Dabrowski, B. Suchońska, R. Kowalczyk, E. Nowacka, B. Kociszewska-Najman, B. Pietrzak, P. Malkowski, M. Wielgos, Pregnancy and delivery in women with esophageal varices due to hepatic vein thrombosis, The Journal of Maternal-Fetal & Neonatal Medicine, 2015, 28, 2, 177CrossRef
- Julien Bissonnette, François Durand, Emmanuelle de Raucourt, Pierre-François Ceccaldi, Aurélie Plessier, Dominique Valla, Pierre-Emmanuel Rautou, Pregnancy and Vascular Liver Disease, Journal of Clinical and Experimental Hepatology, 2015, 5, 1, 41CrossRef
- Nicole Banks, Joy Bryant, Roxanne Fischer, Marjan Huizing, William A. Gahl, Meral Gunay-Aygun, Pregnancy in autosomal recessive polycystic kidney disease, Archives of Gynecology and Obstetrics, 2015, 291, 3, 705CrossRef
- C. J. van der Woude, H. J. Metselaar, S. Danese, Management of gastrointestinal and liver diseases during pregnancy, Gut, 2014, 63, 6, 1014CrossRef
- Neelam Aggarwal, Neha Negi, Aakash Aggarwal, Vijay Bodh, Radha K. Dhiman, Pregnancy with Portal Hypertension, Journal of Clinical and Experimental Hepatology, 2014, 4, 2, 163CrossRef
- Fabiana Savoia, Cinzia Ferrara, Anna Sansone, Giuseppe Bifulco, Carmine Nappi, Costantino Di Carlo, Portal Cavernoma during Pregnancy, Case Reports in Obstetrics and Gynecology, 2013, 2013, 1CrossRef
- Neelam Aggarwal, Seema Chopra, Ainharan Raveendran, Vanita Suri, Radha Krishan Dhiman, Yogesh Kumar Chawla, Extra hepatic portal vein obstruction and pregnancy outcome: Largest reported experience, Journal of Obstetrics and Gynaecology Research, 2011, 37, 6, 575Wiley Online Library
- Richard C. Britton Pregnancy and esophageal varices The American Journal of Surgery Volume 143, Issue 4, April 1982, Pages 421-425 Volume 22, Issue 1
- D’Amico G et al: The treatment of portal hypertension: A meta-analytic review Hepatol July 1995 Pages 332–354
- Rössle M, Richter GM, Nöldge G, Palmaz JC, Wenz W, Gerok W, New non-operative treatment for variceal haemorrhage, in Lancet, vol. 2, nº 8655, 1989, p. 153, PMID 2567908.
- ^ What You Need to Know about the Transjugular Intrahepatic Portosystemic Shunt (TIPS)., Cleveland Clinic.
- ^ Guevara M, Rodés J, Hepatorenal syndrome, in Int. J. Biochem. Cell Biol., vol. 37, nº 1, 2005, pp. 22–6, DOI:10.1016/j.biocel.2004.06.007, PMID 15381144.
- ^ Rossle M, Piotraschke J. Transjugular intrahepatic portosystemic shunt and hepatic encephalopathy. Dig Dis 1996; 14:12–19.
- ^ Mayan H, Kantor R, Rimon U, Golubev N, Heyman Z, Goshen E, Shalmon B, Weiss P.: “Fatal liver infarction after transjugular intrahepatic portosystemic shunt procedure.” Liver, 2001;21(5):361-4.
- ^ Mallavarapu RK, Grimsley EW, Incarcerated umbilical hernia after transjugular intrahepatic portosystemic shunt procedure for refractory ascites, in Clin. Gastroenterol. Hepatol., vol. 5, nº 9, 2007, pp. A26, DOI:10.1016/j.cgh.2007.07.018, PMID 17825762.
- Azene EM, Hong K. Transjugular intrahepatic portosystemic shunt. In: Cameron JL, Cameron AM, eds. Current Surgical Therapy. 11th ed. Philadelphia, PA: 2014.
- Brooks MD, Li C. Transjugular intrahepatic portosystemic shunt. In: Mauro MA, Murphy KPJ, Thomson KR, Venbrux AC, Morgan RA, eds. Image-Guided Interventions. 2nd ed. Philadelphia, PA: Elsevier Saunders; 2014:chap 112.
- Garcia-Tsao G, Sanyal AJ, Grace ND, Carey WD; Practice Guidelines Committee of American Association for Study of Liver Diseases; Practice Parameters Committee of American College of Gastroenterology. Prevention and management of gastroesophageal varices and variceal hemorrhage in cirrhosis. Am J Gastroenterol. 2007;102:2086-2102.
- Garcia-Tsao G. Cirrhosis and its sequelae. In: Goldman L, Schafer AI, eds. Cecil Medicine. 24th ed. Philadelphia, Pa: Saunders Elsevier; 2011:chap 156.
- Shaheen NJ, Stuart E, Schmitz SM, Mitchell KL, Fried MW, Zacks S, Russo MW, Galanko J, Shrestha R. Pantoprazole reduces the size of postbanding ulcers after variceal band ligation: a randomized, controlled trial. Hepatology 2005;41:588–594.
- Lo G-H, Chen W-C, Chen M-H, Hsu P-I, Lin C-K, Tsai WL, Lai K-H. A prospective, randomized trial of endoscopic variceal ligation versus nadolol and isosorbide mononitrate for the prevention of esophageal variceal rebleeding. Gastroenterology 2002;123:728–734.
- Patch D, Goulis J, Gerunda G, Greenslade L, Merkel C, Burroughs AK. A randomized controlled trial of medical therapy versus endoscopic ligation for the prevention of variceal rebleeding in patients with cirrhosis. Gastroenterology 2002;123:1013–1019.
- Groszmann RJ, Garcia-Tsao G. Endoscopic variceal banding vs pharmacological therapy for the prevention of recurrent variceal hemorrhage: What makes the difference? Gastroenterology 2002;123:1388–1391.
- Lo GH, Lai KH, Cheng JS, Chen MH, Huang HC, Hsu PI, Lin CK. Endoscopic variceal ligation plus nadolol and sucralfate compared with ligation alone for the prevention of variceal rebleeding: a prospective, randomized trial. Hepatology 2000;32:461–465.
- De la Pena J, Brullet E, Sanchez-Hernandez E, Rivero M, Vergara M, Martin-Lorente JL, Garcia SC. Variceal ligation plus nadolol compared with ligation for prophylaxis of variceal rebleeding: a multicenter trial. Hepatology 2005;41:572–578.
- Bureau C, Peron JM, Alric L, Morales J, Sanchez J, Barange K, Payen JL, Vinel JP. “A La Carte” treatment of portal hypertension: Adapting medical therapy to hemodynamic response for the prevention of bleeding. Hepatology 2002;36:1361–1366.
- Gonzalez A, Augustin S, Perez M, Dot J, Saperas E, Tomasello A, Segarra A, Armengol JR, Malagelada JR, Esteban R, Guardia J, Genesca J. Hemodynamic response-guided therapy for prevention of variceal rebleeding: an uncontrolled pilot study. Hepatology 2006;44:806–812.
- Conn HO. The rational evaluation and management of portal hypertension. In: Schaffner F, Sherlock S, Leevy CM. eds. The Liver and its Diseases. New York: Intercontinental, 1974: 289–306.
- Grace ND, Conn HO, Resnick RH, Groszmann RJ, Atterbury CE, Wright SC, Gusberg RJ, Vollman R, Garcia-Tsao G, Fisher RL, O’Hara E, McDermott WV, Maselli JP, Widrich W, Matloff DS, Horst D, Banks N, Alberts J. Distal splenorenal vs portal-systemic shunts after hemorrhage from varices: A randomized clinical trial. Hepatology 1988;8:1475–1481.
- Luca A, D’Amico G, LaGalla R, Midiri M, Morabito A, Pagliaro L. TIPS for prevention of recurrent bleeding in patients with cirrhosis: meta-analysis of randomized clinical trials. Radiology 1999;212:411–421.
- Papatheodoridis GV, Goulis J, Leandro G, Patch D, Burroughs AK. Transjugular intrahepatic portsystemic shunt compared with endoscopic treatment for prevention of variceal rebleeding. A meta-analysis. Hepatology 1999;30:612–622
- Escorsell A, Banares R, Garcia-Pagan JC, Gilabert R, Moitinho E, Piqueras B, Bru C, Echenagusia A, Granados A, Bosch J. TIPS versus drug therapy in preventing variceal rebleeding in advanced cirrhosis: a randomized controlled trial. Hepatology 2002;35:385–392.
- Henderson JM, Boyer TD, Kutner MH, Galloway JR, Rikkers LF, Jeffers LJ, Abu-Elmagd K, Connor J. Distal splenorenal shunt versus transjugular intrahepatic portal systematic shunt for variceal bleeding: a randomized trial. Gastroenterology 2006;130:1643–1651.
- Bureau C, Garcia-Pagan JC, Otal P, Pomier-Layrargues G, Chabbert V, Cortez C, Perreault P, Peron JM, Abraldes JG, Bouchard L, Bilbao JI, Bosch J, Rousseau H, Vinel JP. Improved clinical outcome using polytetrafluoroethylenecoated stents for TIPS: results of a randomized study. Gastroenterology 2004;126:469–475.
- Singh P, Pooran N, Indaram A, Bank S. Combined ligation and sclerotherapy versus ligation alone for secondary prophylaxis of esophageal variceal bleeding: A meta-analysis. Am J Gastroenterol 2002;97:623–629.
- Karsan HA, Morton SC, Shekelle PG, Spiegel BM, Suttorp MJ, Edelstein MA, Gralnek IM. Combination endoscopic band ligation and sclerotherapy compared with endoscopic band ligation alone for the secondary prophylaxis of esophageal variceal hemorrhage: a meta-analysis. Dig Dis Sci 2005;50:399–406.