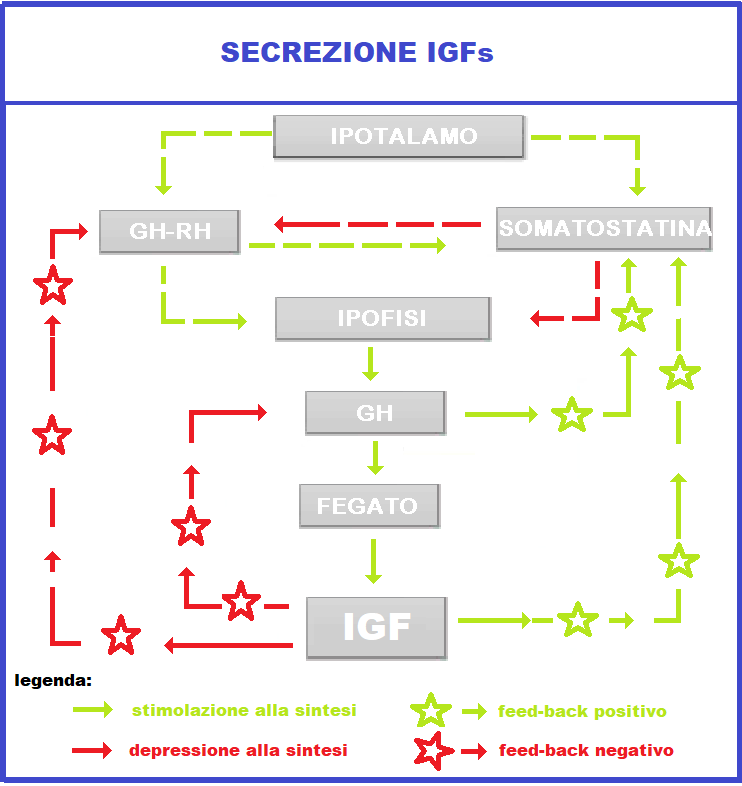
Le IGFs (Insulin-like Growth Factor I-II), conosciute anche con il nome di somatomedine, sono proteine con una struttura molecolare molto simile all’insulina. La principale azione delle IGFs è quella di mediare l’attività del GH, costituiscono il “braccio armato” dell’ormone della crescita..
La loro produzione è ubiquitaria ma in modo preponderante la secrezione avviene nel fegato (75%) sotto lo stimolo dell’ormone della crescita (GH) ed è soggetta a diversi meccanismi incrociati di feed-back positivi e negativi. L’IGF esercita feed-back negativo sulla secrezione ipotalamica di GH sia mediante la stimolazione della secrezione di somatostatina sia direttamente a livello ipofisario.
MECCANISMO D’AZIONE DELLE IGFs
IGFs agiscono legandosi a specifici recettori cellulari (IGF1-R e IGF2-R) sugli organi target e viaggiano in circolo trasportati dalle proteine IGF-BP, una famiglia di sei proteine (classificate da 1 a 6). La IGFBP-3 lega il 90% di IGF-I circolante mentre le altre cinque IGF-BP (1,2,4,5) legano il restante 10% di IGF-I. Gli enzimi che catabolizzano le IGF appartengono alla famiglia delle proteasi; queste ultime in circolo viaggiano associate alle IGF-BP.
- Essenzialmente le IGFs hanno una attività favorente la proteosintesi in simbiosi con il GH (asse GH-IGF); quindi favoriscono la crescita e sviluppo dell’organismo e inibiscono l’apoptosi cellulare di vari organi specialmente cerebrali e nervosi. È stato visto infatti che le malattie neurodegenerative si accompagnano spesso a carenza di somatotropina e IGF-1 (4) e che l’uso di IGF-1 stimola le connessioni neuronali, inibisce la morte dei neuroni e in generale dà grandi benefici ai malati di malattie neurodegenerative compresa la SLA (5). Purtroppo l’elevato costo dei preparati farmaceutici attualmente in commercio ne limita molto le applicazioni cliniche.
- IGF possiedono proprietà anaboliche, antiossidanti, antinfiammatorie e citoprotettive.
- Stimolano l’attività dei condrociti nella sintesi della cartilagine, e degli osteoblasti aumentando il trofismo osseo.
- favoriscono lo smaltimento del tessuto adiposo in eccesso mediante lipolisi

- migliorano la sintesi di DNA, RNA, collagene ed acido ialuronico, grazie allo stimolo sull’azione dei fibroblasti.
- esplicano attività antiandrogena mediante diminuzione della 5-α-reduttasi, che trasforma il testosterone nel più potente DHT d(diidrotestosterone) e depressione dei recettori per gli gli androgeni; ma a livello ovarico favoriscono la secrezione degli androgeni come pure la secrezione del DHEA a livello surrenalico. Anzi che l’azione favorente la proteosintesi sia modulata proprio dal DHEA.
- deprimono l’insulino-resistenza migliorando la sensibilità dei recettori insulinici e relativo uptake del glucosio a livello dei muscoli scheletrici con conseguente blocco o diminuzione del circolo vizioso iperglicemia ⇒ iperinsulinemia ⇒ esaurimento delle cellule ß del pancreas ⇒ diabete II.
- stimolano la produzione di ossido nitrico (NO) con effetto vasodilatatorio periferico di diversi distretti come il tessuto glomerulare, ovarico e testicolare migliorandone microcircolo e funzionalità.
- Migliorano il fluid shear stress con effetto antitrombotico e antiaterosclerotico
- Effetto anti-age – Nel soggetto anziano diminuiti livelli di IGF-1 sono stati associati a una ridotta aspettativa di vita suggerendo una relazione inversa IGF-I e mortalità. Tale effetto sembra esplicarsi tramite effetti protettivi sui mitocondri preservandoli dal danno ossidativo generato dall’aumento del metabolismo, aumentando la sintesi di ATP e riducendo la produzione intramitocondriale di radicali liberi. Alcuni studi hanno infatti mostrato un’associazione tra bassi livelli di IGF-1 e aumentato rischio di malattie cardiovascolari. Sembrerebbe esistere un set-point ottimale tra le modificazioni dell’attività biologica dell’asse GH-IGF e longevità.
- Rischio cancro – molti studi epidemiologici hanno dimostrato una relazione positiva tra alti livelli di IGF, basse concentrazioni di IGF-BP3 e rischio di neoplasie specialmente a livello di prostata, mammella, colon-retto, e polmone. Il rischio cancro è dovuto alla forte attività mitogena e antiapoptotica propria dell’IGF.
Concentrazioni sieriche IGFs – Le IGFs hanno un’emivita di 8-10 ore e non sono soggette a variazioni circadiane né all’effetto di stress di qualsiasi tipo o altri fattori estemporanei eccezion fatta per lo stato nutrizionale (1).
- Fisiologicamente i valori più bassi si riscontrano nell’infanzia e nella terza età. Tuttavia il declino legato all’invecchiamento può essere prevenuto da un adeguato livello di attività fisica e da un’alimentazione cautamente iperproteica, ricca di fibre, vegetali e acqua (9,10).
- IGF-II è presente soprattutto nella vita fetale ed è solo parzialmente GH dipendente.
- IGF-I è massimo in pubertà e strettamente GH dipendente. Un alto dosaggio di IGF nel sangue di un bambino è sinonimo di elevato Quoziente Intellettivo (1).
- Aumento fisiologico dei livelli sierici di IGF si verificano in gravidanza e in soggetti con dieta ad alto contenuto energetico.
VALORI FISIOLOGICI SIERICI DI IGF-I (ng/ml) |
|||
| femmine | maschi | ||
| 1 giorno – 4 anni | 33.5 – 171.8 | 27.4 – 113.5 | |
| 4 – 7 anni |
79.8 – 244 |
54.9 – 206.4 | |
| 7 – 10 anni | 87.4 – 399.3 | 85.2 – 248.8 | |
| 10 – 14 anni |
188.4 – 509.9 | 115.4 – 498.2 | |
| 14 – 19 anni | 267.5 – 470.8 | 247.3 – 481.7 | |
| 19 – 23 anni |
149.4 – 332.3 |
187.9 – 400 | |
| 23 – 38 anni | 107.8 – 246.7 | 96.4 – 227.8 | |
| 38 – 53 anni |
92.7 – 244.6 |
8.3 – 209.9 | |
| >53 anni | 40.4 – 156.2 |
54.6 – 185.7 | |
Il bodybuilding sembra l’attività più indicata per aumentare la secrezione e gli effetti benefici dell’IGF-1. Nello specifico il massimo stimolo si ottiene con allenamenti ad alta intensità che non superino i 45 minuti. Tale tipologia di allenamento può tuttavia essere praticata soltanto da atleti sani ed esperti, mentre è sconsigliata per diabetici, ipertesi, cardiopatici e per chi soffre di seri problemi articolari. In questi casi sono più indicate attività di tipo aerobico come il nuoto, jogging, il ciclismo e le passeggiate che, pur avendo un’efficacia minore, contribuiscono senza dubbio a rallentarne il processo di invecchiamento.
Dieta e IGF – Per aumentare la secrezione di somatomedine è consigliata inoltre un’alimentazione ricca di acqua, fibre e vitamine, astinenza da alcolici, droghe e fumo, l’osservanza del giusto periodo di riposo notturno e la riduzione dello stress. Quando è presente una restrizione calorica, i mammiferi sintetizzano meno IGF-1 e la sua sintesi nel fegato è refrattaria alla stimolazione del GH. Questo processo funziona per limitare la crescita e la sintesi proteica quando la disponibilità di nutrienti è compromessa. Dopo un pasto, la risposta al GH e la sintesi dell’IGF-1 vengono ripristinate. Quando vengono ingeriti carboidrati inadeguati, la diminuzione della concentrazione di insulina nella vena porta induce una riduzione della sintesi di IGF-1 da parte del fegato.
La concentrazione di IGF-1 è piu bassa nelle femmine rispetto ai maschi di pari età per una resistenza epatica all’azione del GH indotta da estrogeni. La concentrazione di GH a sua volta varia in base al ciclo mestruale, raggiungendo valori più elevati in fase ovulatoria (6-8).
Il dosaggio di GH e IGF-1 è limitato da problemi di variabilità e interpretazione dei risultati. Le cause possono essere molteplici: tipo di dosaggio e modalità di valutazione, cut-off impiegati, patologie che modificano le concentrazioni di GH o di IGF-1, errore nel timing del dosaggio, terapie concomitanti.
Deficit di IGFs e carenza o ridotta funzionalità dei suoi recettori, si riscontrano nei ritardi di crescita (nanismi), in casi di insufficienza epatica, alcoolismo, terapia estrogenica, nell’ipotiroidismo, ipopituarismo, nei diabetici I-II e nelle pazienti PCOS, cirrosi epatica, invecchiamento comprese le malattie cardiovascolari e neurologiche legate all’età, sindrome metabolica (MetS) e più recentemente, restrizione della crescita intrauterina (IUGR).
Sindrome di Laron – Zvi Laron descrisse per primo in alcune famiglie israeliane una forma di GRAVE RITARDO STATURALE armonico, analogo al nanismo da deficit di GH ma caratterizzato da alte concentrazioni di GH e da insufficienza della terapia col GH stesso. La sindrome di Laron o nanismo di Laron è una malattia genetica autosomica recessiva, vale a dire che, per manifestarsi, è necessario che siano alterati tutti e due i geni facenti parte della coppia presente nel corredo genetico dell’individuo. E’ caratterizzata dalla mancata risposta dei tessuti alla somatotropina, a causa di una mutazione dei recettori per IGFs. È causa di bassa statura, ma anche di bassa incidenza di diabete e neoplasie. Il gene che codifica l’IGF è posto nel CROMOSOMA 12. Le persone affette da S. di Laron presentano, oltre alla bassa statura idiopatica, particolari riformismi del capo: bozze frontali prominenti, naso a sella, orbite profonde, neurocranio prevalente sullo splancnocranio. Lo sviluppo motorio è più lento, probabilmente per la ridotta componente muscolare. Le acquisizioni cognitive sono compromesse se il deficit di IGFs inizia dalla vita intrauterina.
Sindrome metabolica (MetS) e IGF – la diagnosi di MetS viene effettuata quando sono presenti 3 dei seguenti 5 fattori di rischio: circonferenza della vita aumentata rispetto ai criteri specifici della popolazione locale; trigliceridi elevati (≥150 mg/dL), riduzione delle lipoproteine ad alta densità (HDL) (<40 mg / dL negli uomini e 50 mg / dL nelle donne), pressione arteriosa elevata (sistolica >140 mm Hg e diastolica >85 mmHg) e glicemia elevata a digiuno (>100 mg / dL). La MetS sta aumentando in tutto il mondo e sembra sia correlato alla progressiva occidentalizzazione delle abitudini di vita e alimentazione.
Ipersecrezione di IGF-I – Aumento patologico di IGF-I si verifica per acromegalia e iperandrogenemia.
METABOLISMO: le IGFs sono degradate dalle proteasi
IGFs ed OVAIO –
Anche le cellule della granulosa ovarica presiedono alla sintesi delle IGF. L’IGF promuove la replicazione delle stesse cellule della granulosa ed anche la trasformazione di esse in altri tipi di cellule ovariche.
L’IGF a livello ovarico promuove un’azione FSH-sinergica nel processo steroidogenetico oltre ad esplicare un’azione antiandrogena (2).
Un’alta concentrazione di IGF-BP può inibire il normale meccanismo steroidogenetico per blocco dell’azione delle IGF e conseguente anovulazione e PCOS (3-5).
Potenziali opzioni terapeutiche – sembrano essere limitate a quegli stati provati di deficit di IGF-I locale o sistemico piuttosto che aumentarne la concentrazione sierica al di sopra dei normali livelli fisiologici.
References:
- Nestler JE, Powers LP, Matt DW, Steingold KA, Plymate SR, Rittmaster RS, et al. A direct effect of hyperinsulinemia on serum sex hormone–binding globulin levels, Barnes R, Rosenfield RL: “Polycystic ovary syndrome in obese women with the polycystic ovary syndrome. J Clin Endocrinol Metab. 1991;72:83–89
- Nestler JE. Role of hyperinsulinemia in the pathogenesis of the polycystic ovary syndrome, and its clinical implications. Semin Reprod Endocrinol 1997;15(2):111-22
- Adashi E. Y Insulin-like growth factors as intraovarian regulators of granulosa cell growth and function. Endocr Rev 1985; 6:400-20.
- Yoshimura Y. : “Insulin-like growth factors and ovarian physiology”. J Obstet Gynaecol Res. 1998 Oct;24(5):305-23
- Adashi EY, Resnick CE, D’Ercole AJ, Svoboda ME, Van Wyk JJ. Insulin-like growth factors as intraovarian regulators of granulose cell growth and function. Endocrinol Rev. 1985;6:400–420
- Faria AC et al. 1992, Clin Endocrinol 36(6):591–596 Roelfsema F. et al. 2016. Neuroendocrinology 103(3–4):335–344
- Freda PU, et al. Journal of Clinical Endocrinology and Metabolism. 2004; 89:495–500.
- Freda P. U. et al. Clin Endocrinol (Oxf). 2009 August ; 71(2): 166–170.
- Sherlock M, Toogood AA. Aging and the growth hormone/insulin like growth factor-I axis. Pituitary 2007;10:18-203.
- Felsing NE, Brasel JA, Cooper DM. Effect of low and high intensity exercise on circulating growth hormone in men. J Clin Endocrinol Metab 1992;75:157-62.