Ultimo aggiornamento 2022-04-07 20:32:50
L’isterectomia è uno degli interventi chirurgici maggiori più frequentemente eseguiti nel mondo occidentale, secondo solo al taglio cesareo; più frequente negli USA che in Scandinavia o in Inghilterra, più frequente nelle donne di non elevata condizione socio-economica e, negli USA, in quelle di colore. I chirurghi uomini risultano più interventisti delle donne (1).
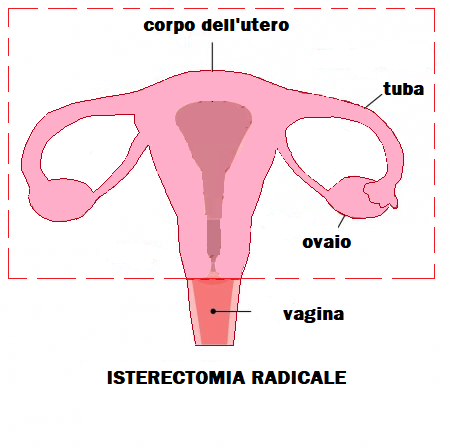
LE INDICAZIONI ALL’ISTERECTOMIA
VIE DI ACCESSO ALL’ISTERECTOMIA:
Ancora recentemente le vie di approccio per l’intervento di isterectomia erano due: quella laparotomica e quella vaginale con una percentuale del 66.3% e del 33.7% (2).
La via vaginale comporta vantaggi rispetto alla via addominale in termini di trauma chirurgico, ripresa funzionale post-operatoria, tempi di degenza e di complicazioni e morbosità post-operatoria. La via vaginale è però controindicata in presenza di utero di grandi dimensioni (ø >10 cm) e in caso di nulliparità, fissità uterina, patologia annessiale, anamnesi positiva per infezioni genito-pelviche, endometriosi e precedenti interventi chirurgici addominali. La via vaginale è utilizzata nel 91.9% dei casi di prolasso (2). L’aditus alla via vaginale cresce con il progredire dell’età delle pazienti (2,3).
Il più recente approccio all’isterectomia è quello endoscopico. Nel 1989 Hang Reich ha descritto la prima isterectomia eseguita per via laparoscopica: l’entusiasmo che ha fatto seguito a questo traguardo ha condotto alla nascita di numerosi Centri di “advanced laparoscopy” che praticano l’isterectomia laparoscopica (15).
| Tab. 2 – Varianti tecniche e vie di accesso per isterectomia | |
| VARIANTI TECNICHE | VIE DI ACCESSO |
| Totale | Addominale |
| Vaginale | |
| LPS | |
| Subtotale | Addominale |
| LPS | |
| Radicale | Addominale |
| Vaginale | |
| LPS + vaginale | |
Tuttavia la sicurezza e l’efficacia rispetto alle tecniche classiche dell’uso indiscriminato delle procedure endoscopiche rimangono in gran parte da determinare: le complicazioni non sono certo azzerate e i tempi anestesiologici di molto allungati; almeno nel 10-25% dei casi (a seconda dell’abilità degli operatori) Inoltre è tecnicamente impossibile effettuare una conversione chirurgica nella classica via vaginale o laparotomica. Non è ancora, quindi, il caso di pronunciare il “necrologio” della chirurgia classica; piuttosto può essere messo in discussione il modo classico di intendere la chirurgia: i vantaggi della chirurgia microinvasiva sembrano attualmente quelli di far aumentare le isterectomie eseguite vaginalmente (isterectomia vaginale assistita laparoscopicamente) nei casi in cui la via vaginale non sarebbe indicata o sarebbe con molta difficoltà, proponibile. Questo dovrebbe comportare una minore incidenza delle complicanze e una minor durata dell’ospedalizzazione. Questa strategia chirurgica permetterà di effettuare per via laparoscopica un’adesiolisi e consentirà l’asportazione dell’utero per via vaginale. Viceversa, in caso di aderenze particolarmente tenaci per le quali un’adesiolisi endoscopica risulterebbe pericolosa o impossibile, questa attitudine permetterà, d’emblèe di porre indicazione alla via addominale evitando così di intraprendere un’isterectomia per via vaginale in condizioni sfavorevoli
LAPAROISTERECTOMIA: TECNICA CHIRURGICA
La paziente è sistemata sul letto operatorio in posizione litotomica dorsale. Una esplorazione ginecologica viene effettuata in anestesia. Si pone quindi la paziente in posizione supina ed lieve Trendelenburg (15°).
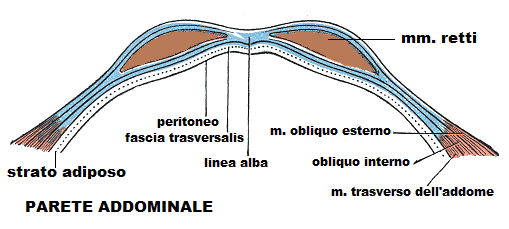
ll sottocute e l’aponeurosi anteriore dei retti vengono incisi per alcuni centimetri e quindi divaricati manualmente insieme ai muscoli retti addominali anteriori. Per avere maggiore spazio si può procedere alla divaricazione del muscolo piramidale in prossimità del margine superiore pubico. Il m. piramidale ha origine dalla faccia anteriore del ramo superiore del pube, tra il tubercolo e la sinfisi, e si porta in alto e medialmente per prendere inserzione sulla linea alba. Contraendosi mette in tensione la linea alba. E’ innervato dall’ultmo nervo intercostale.
Con la divaricazione manuale si evita di lacerare il nervo ileo-ipogastrico, il nervo ileo-inguinale e il n. cutaneo femorale (foto a lato), i muscoli obliquo esterno, obliquo interno e trasverso ed i vasi epigastrici.
Fascia trasversalis: si incide con il bisturi la fascia trasversalis per alcuni cm; si continua l’incisione trasversale della stessa mediante forbici di Metzenbaum.
Peritoneo parietale: sottile strato di sierosa separato dalla fascia trasversalis da un sottile strato di grasso, riveste le pareti di tutta la cavità addomino-pelvica. Per inciderlo, l’operatore lo pinzetta delicatamente a livello dell’uraco, lo solleva in alto e lo palpa fra le dita per evidenziare eventuali aderenze dell’omento o di visceri addominali. Quindi l’aiuto operatore pinzetta un punto del foglio peritoneale precedentemente sollevato dall’operatore che può ora procedere all’incisione del peritoneo nel punto più vicino alla pinza manovrata dall’aiuto. Sulla guida di indice e medio infilati sotto il peritoneo, quest’ultimo viene sezionato per la larghezza desiderata con forbici di Mayo-Harrongton curva.
un punto del foglio peritoneale precedentemente sollevato dall’operatore che può ora procedere all’incisione del peritoneo nel punto più vicino alla pinza manovrata dall’aiuto. Sulla guida di indice e medio infilati sotto il peritoneo, quest’ultimo viene sezionato per la larghezza desiderata con forbici di Mayo-Harrongton curva.
Dopo l’apertura del peritoneo
- divaricazione del campo operatorio mediante divaricatore di Balfour a tre pacche o retrattore addominale
 di Kirchner a 4 valve
di Kirchner a 4 valve - Sollevare in alto l’utero mediante elicoide di Doyen inserito sul fondo dell’utero o con l’applicazione di un grosso filo di sutura sul fondo (v. disegno) o mediante 2 lunghi Kocher inseriti sugli annessi all’estremo prossimale.
- Pinzettamento, coagulazione e sezione dei ligamenti rotondi; sutura dei capi distali; sui capi prossimali si lasciano i Koker che aiuteranno a mobilizzare l’utero.
- Apertura pagina anteriore del legamento largo, visualizzazione e lateralizzazione dell’uretere.
- Apertura pagina posteriore legamento largo
Nel tessuto areolare lasso del lig. largo, sul fondo, si evidenzia, la biforcazione dell’a. iliaca comune e l’uretere che scavalca l’a. iliaca comune poco prima della biforcazione dell’arteria stessa.
- si reperta l’a. iliaca esterna che decorre lungo la faccia mediale del m. psoas.
- Scollamento plica vescica-uterina con forbici di Mezenbaum
- Resezione dell’infundibolo pelvico. Si evidenzia l’uretere e lo si sposta medialmente prima di procedere a
- forcipessura, resezione e legatura di arteria e vene uterine in corrispondenza dell’angolo supero-laterale dell’utero, 1 cm prima che l’a. uterina si divida nei suoi rami terminali uterini e dopo l’origine dell’a. vaginale. Se i vasi non sono visibili, per evidenziarli basterà un modesto scollamento con tampone montato del margine uterino.
- Preparazione dei legamenti utero-sacrali
- Pinzettamento, Recisione e legatura dei ligamenti utero-sacrali
- Pinzettamento, recisione e legatura dei lig cardinali; recisione a 2-3 cm dall’utero tenendo ben lontani la vescica e l’uretere.
RIMOZIONE DELL’UTERO:
- si utilizzano 2 pinze di Faure o robuste pinze di Cocker curve per prendere per gli angoli vaginali il più possibile vicino alla giunzione vagino-cervicale (in questo modo si clampa la vaginale superiore). Insione fra le due pinze ed apertura della vagina. si ripete l’operazione dall’altro lato. Si incide di continuo la fascia vaginale con forbici curve di Metzembaum o con bisturi elettrico.
Variante intrafasciale: la fascia cervicale circonda il collo dell’utero. Anteriormente prende rapporto con la fascia vescicale; posteriorment invece è separata dalla fascia rettale da tessuto connettivo lasso di riempimento. Sulla fascia cervicale si inseriscono: lateralmente i ligamenti cardinali di Mackenrodt (o parametrio laterale); anteriormente il fascio vescico-cervicale del ligamento pubo-cervicale (o pilastro vescicale o parametrio anteriore); posteriormente i ligamenti utero-sacrali (o pilastro rettale) che, nell’insieme, realizzano una travatura di sostegno per l’utero e per il terzo superiore della vagina. Da queste premesse anatomo-funzionali si evince il razionale dell’impiego di una tecnica di isterectomia intrafasciale in cui la fascia cervicale viene incisa con elettrobisturi circolarmente a livello istmico iniziando al disopra della legatura inferiore dei vasi uterini e quindi sopra i lig. utero-sacrali ed infine continuata circolarmente scollando la fascia cervicale dal sottostante tessuto muscolare sino ad ottenere un manicotto di tessuto fibroso che mantiene inalterate le connessioni con il connettivo endopelvico circostante. In tal modo si realizza la migliore prevenzione possibile del prolasso della cupola vaginale e della vescica. Inoltre, all’esterno di questo manicotto vengono preservati i rami cervicali e vaginali dell’arteria uterina e, data la maggiore distanza tra piano di dissezione ed uretere, è meno probabile causare danni a questa struttura.
SUTURA CUPOLA VAGINALE e PERITONEIZZAZIONE
- Un punto a 8 ai due lati dove sono i 2 grossi cocker
- La rima vaginale è accostata con pinze di Heaney
- Sutura a punti staccati a X
- I capi della sutura dei ligamenti cardinali o dei ligamenti rotondi vengono annodati con quelli della cupola vaginale (colposospensione sec. Mc Call)
- La cupola vaginale può essere lasciata aperta per facilitare il monitorraggio su eventuali emorragie post-chirurgiche e per favorire il drenaggio delle secrezioni e l’espulsione dei fili di sutura dopo alcuni giorni. In tal caso occorre suturare i margini vaginali ad orletto.
Irrigazione e lavaggio della cavità addominale (washing peritoneale) che potrà essere inviato all’esame citologico in caso di lesioni sospette.
Sospensione delle ovaie alla parete addominale se non sono state asportate.
Non suturiamo il peritoneo anteriore.
anteriore.
Sutura fascia: con filo tipo “Vicryl” o “Vicryl Plus” n. 2, staccati. ad X o Blair-Donati, ben serrati con la tensione giusta in modo da evitare spazi morti ma non eccessivamente stretti per evitare fenomeni necrotici, simmetrici, distanziari di 1 cm, che comprendano la stessa quantità di tessuto e a margini dritti in modo che i lembi si ritrovino affrontati direttamente.
Il punto ad X è un punto doppio in cui i due fori di entrata sono asimmetrici rispetto a quelli di uscita in modo che il filo forma una X orizzontale.
Non suturare il sottocute può servire ad evitare fenomeni colliquativi
Vicryl (poliglattina 910) è una sutura formata da materiale sintetico, ac. poliglicolico (ac. lattico 10% + ac. glicolico 90%), intrecciato. Mantiene la sutura in tensione stenza alla trazione per circa 3-4 settimane, ed è completamente assorbito mediante idrolisi entro 60 giorni. E’ impregnato con triclosan, antibatterico ad ampio spettro. Altre suture a base di acido poliglicolico sono Surgicryl, Biovek, Visorb, Polysorb e Dexon. Il “Vicryl Plus” è una sutura di nuova concezione in cui, nel processo di polimerizzazione, è stato aggiunto il dodecanolo che permette un aumento della resistenza alla tensione del 25%. L’ulteriore processo di lubrificazione superficiale con stearato di calcio permette un facile passaggio attraverso il tessuto, il confezionamento comodo del nodo ed un agevole affondamento dello stesso.